COME FUNZIONA: Caro Visitatore questo sito ha una parte accessibile solo previa iscrizione (FORUM) e accettazione delle regole di uso e una parte informativa accessibile a tutti in cui puoi trovare gli articoli scritti da medici o utenti del nostro forum. NOTA BENE: I COMMENTI AGLI ARTICOLI PUBBLICI SONO VISIBILI A TUTTI.
Se vorrai confrontarti o portare la tua esperienza potrai anche iscriverti al nostro forum, che è riservato e accessibile solo sotto utente e password al fine di osservare le regole di base di privacy dei partecipanti, oppure puoi consultare gli articoli liberamente.
SE TI REGISTRI COME MEMBRO DEL FORUM DI FIBRILLAZIONEATRIALE.IT, POTRAI CONSULTARE ANCHE L'ELENCO DEGLI INDIRIZZI DEI MEDICI CHE GENTILMENTE SI SONO RESI DISPONIBILI A RISPONDERE VIA MAIL.
Altro...
Consigli prenotazione TAC Cardiaca / Coronarica
Consigli prenotazione TAC Cardiaca / Coronarica
Prenotare una TAC cardiaca/coronarica in Lombardia non è semplice.
Non tutte le strutture la fanno, molte hanno liste d'attesa di diversi mesi, altre fanno l'esame solo a chi è già in cura presso di loro, altre ancora solo in privato.
L'esame NON è prenotabile tramite callcenter regionale (numero verde) ma si viene generalmente invitati ad andare di persona ai cup delle varie strutture in quanto ogni struttura ha una gestione/organizzazione autonoma per la prenotazione di questo esame.
Tra le varie strutture contattate nel mese di settembre 2017, elenco quelle NON viene fatto questo esame, in modo che possiate evitare di perdere tempo a contattarle:
POLITERAPICO POLIDIAGNOSTICO Monza
Policlinico San Marco - Bergamo
Studio Radiologico Bernasconi di Seregno
CRC Garbagnate
Centro fisioterapico Gorle
Studio Radiologico Parabiago
Habilita Sarnico
by Silvia F. Club cuori capricciosi
Consigli: Risonanza Magnetica per portatori di Pacemaker compatibile
Consigli prenotazione Risonanza Magnetica per portatori di Pacemaker compatibile (es. Pacemaker St. Jude Medical)
Generalmente chi è portatore di pacemaker non può sottoporsi a Risonanza Magnetica.
Ci sono però dei modelli di PM compatibili con questo tipo di esame, come per esempio il PM della St. Jude Medical.
Purtroppo molte strutture sanitarie non sono a conoscenza di questi dispositivi compatibili e spesso si rifiutano di farvi l'esame.
In pratica, per poter fare la RNM ad un portatore di PM compatibile, al momento dell'esame deve essere presente un cardiologo che imposta (tramite computer) il PM in “modalità risonanza” (una sorta di “modalità aereo” di smartphone e tablet) e disabilita tale modalità al termine dell'esame.
Tra le varie strutture che ho contattato, Humanitas è in grado di fare questo.
Maggiori info:
By Silvia F. club cuori capricciosi
ESTRATTO LINEE GUIDA 2016 FIBRILLAZIONE ATRIALE
CARISSIMI AMICI, COME PROMESSO ECCO A VOI UN ESTRATTO DELLE LINEE GUIDA IN VERSIONE ITALIANA. L'estratto è stato supervisionato dal dott. Stefano Benussi che ringrazio moltissimo da parte di tutti, senza nulla togliere anche a Elena Pucitta e a tutti i membri dello staff di cuori capricciosi, che non si risparmiano mai quando c'e' da dare una mano.
BUONA LETTURA e ricordatevi :
GRUPPO FACEBOOK CUORI CAPRICCIOSI : http://www.fibrillazioneatriale.it/facebook
LINEE GUIDE ESTRATTO 2016 IN ITALIANO: https://www.fibrillazioneatriale.it/images/pdf/FA_linee_guida_2017_Riccione_ITA_light_rev02
ESC 2016: le novità delle ultime linee guida ESC sulla fibrillazione atriale
Multidisciplinary Arrhythmia Meeting 2016
Multidisciplinary Arrhythmia Meeting: Focus on Atrial Fibrillation Management, to be held in 2 weeks, on 15-16 September, in Zurich.
scarica il file del programma aggiornato cliccando sul link di seguito
ARITMIE: PER SAPERNE DI PIU'
Cari amici ed amiche
Quest'anno a Milano ho organizzatoo un evento importante che interesserà tutti noi che abbiamo problemi di aritmie, infatti Domenica 10 Aprile 2016 alle ore 15 avremo come illustre ospite il Prof. Dott Roberto De Ponti docente di cardiologia dell' Università dell'Insubria e Responsabile del laboratorio di Elettrofisiologia dell'ospedale di Circolo e fondazione Macchi di Varese.
Il medico ci illustrerà le ultime novità in ambito aritmologico e successivamente risponderà alle nostre domande.
L'incontro avverrà presso il CIRCOLO ARCI METISSAGE in via GAETANO DE CASTILLIA 8 angolo via BORSIERI 2 fermata metropolitana LINEA 2 GIOIA A UNA FERMATA DALLA STAZIONE FS DI CENTRALE E DI GARIBALDI.
L'evento sarà preceduto per chi lo desiderasse da un pranzo alle ore 12:30 presso l'OSTERIA BORSIERI di via Borsieri 39 che si trova a circa 300 metri dal circolo sopra nominato al costo di euro 25
Gli interessati possono lasciare la loro adesione all'evento scrivendomi in privato oppure confermando la propria partecipazione in uno dei seguentii gruppi facebook
PASSIONE ECG
CLUB DEI CUORI CAPRICCIOSI
ODDIO N'ALTRA EXTRASISTOLE
SINDROME DI BRUGADA
Vi ringrazio per la cortese collaborazione
Elena Antonioli

LA FIBRILLAZIONE ATRIALE
La fibrillazione atriale (FA) è l'aritmia più comune, ma è anche una delle più difficile da trattare. La sua incidenza è stimata intorno allo 0.4/0.5% della popolazione e cresce con l’aumentare dell'età. Il meccanismo d’innesco della FA comporta un'interazione tra eventi di attivazione elettrica e il substrato endocardico/ miocardico che permette la propagazione e il mantenimento del circuito elettrico anomalo. Il trigger focale più comune di FA sembra essere situato all'interno della cavità atriale del muscolo cardiaco che si estende nelle vene polmonari.
La FA rappresenta la causa di circa un terzo dei ricoveri per disturbi del ritmo cardiaco. I sintomi della FA sono: palpitazioni, ridotta tolleranza allo sforzo e dispnea e, sono principalmente legati a frequenza cardiaca mal controllata o irregolare con conseguente perdita della sincronia nella gittata cardiaca. Quest’ultima risulta perciò diminuita e, può essere dannosa in pazienti con funzionalità cardiaca compromessa. Inoltre, i pazienti con FA sono esposti ad un più alto rischio di ictus e, agli stessi, è particolarmente raccomandato l’utilizzo di anticoagulanti. FA è anche associata ad altre patologie cardiache, come la malattia valvolare cardiaca, insufficienza cardiaca, ipertensione e diabete. È pur vero che episodi di FA possono essere convertiti in ritmo sinusale mediante cardioversione elettrica o farmacologica.
La fibrillazione atriale viene divisa in 3 tipi:
- Parossistica: con una durata di meno di sette giorni e, generalmente, non comporta l’ausilio di cardioversione farmacologica;
- Persistente: dura più di sette giorni e può richiedere l’utilizzo di cardioversione farmacologica o elettrica;
- Permanente: quando l’irregolarità del battito cardiaco atriale si presenta da più di un anno, e richiede il trattamento farmacologico e l’assunzione di anticoagulanti.
Attualmente, le principali indicazioni terapeutiche per il controllo del ritmo sono solo per i pazienti affetti da FA parossistica o persistente. Una strategia di controllo del ritmo avviene inizialmente con il ricorso alla cardioversione farmacologica o elettrica e, successivamente, con un trattamento farmacologico al fine di mantenere il normale ritmo sinusale. Tuttavia, i farmaci antiaritmici spesso non sono efficaci nel mantenimento del ritmo sinusale e, come risultato, si hanno episodi di FA ricorrente. In questo modo, i pazienti con fibrillazione atriale persistente possono subire diversi episodi di cardioversione. I pazienti con fibrillazione atriale parossistica, per definizione, non richiedono la cardioversione, ma possono essere trattati farmacologicamente per prevenire maggiori episodi aritmici.
Il trattamento della fibrillazione atriale permanente si concentra sul controllo della frequenza, utilizzando la terapia farmacologica o l'ablazione del nodo Atrio Ventricolare, seguita da stimolazione ventricolare. Sebbene ablazione del nodo AV produca un miglioramento dei sintomi, essa comporta l’assunzione dell’anticoagulante per tutta la vita (a causa della fibrillazione degli atri) e la perdita della sincronia AV naturale, che porta la dipendenza a vita dal pacemaker.
L’opzione del trattamento farmacologico ad oggi non può essere considerata un metodo curativo, mentre una varietà di procedure ablative sono state studiate come approcci potenzialmente curativi.
ABLAZIONE TRANS CATETERE
Ablazione trans catetere con radiofrequenza, è un’ approccio largamente utilizzato per il trattamento di aritmie sopraventricolari. La fibrillazione atriale nasce spesso da un focus anomalo in prossimità della giunzione tra le vene polmonari e l'atrio sinistro, determina la fattibilità dell’intervento di ablazione.
L’ablazione a radiofrequenza è una tecnica basata sull’utilizzo di un catetere percutaneo, essa è ampiamente utilizzata per una varietà di aritmie, in cui la mappatura intracardiaca identifica una zona focale che è la destinazione di ablazione. La situazione è però più complessa per FA poiché non esiste una sola zona focale, ma più focolai. Alla fine del 1990, il professore Haissaguerre, noto aritmologo francese, dimostrò che la FA più frequentemente nasce da un focus anormale in prossimità della giunzione tra le vene polmonari e l'atrio sinistro. Tali studi hanno costituito un valido fondamento per l’utilizzo delle tecniche di ablazione percutanea più mirate.
La necessità di ripetere le procedure può, in parte dipendere dalle caratteristiche cliniche del paziente (ad esempio età, FA persistente, dilatazione atriale) e il tipo di ablazione iniziale effettuata. Le procedure successive, se necessarie, richiedono generalmente un lasso di tempo più limitato. Ad esempio, nei casi in cui si verificano dei piccoli focus elettrici, a causa di linee di ablazione incomplete, una procedura "ritocco" è fatto per correggere le lacune nell’ablazione originale.
ABLAZIONE CON RADIO FREQUENZA UNIPOLARE
La radio frequenza unipolare è una radiazione non ionica facendo parte del gruppo delle onde elettromagnetiche. Da un punto di vista energetico, avviene che l’azione delle radiazioni elettromagnetiche a contatto con il tessuto biologico, si trasforma in energia termica (calore). La distribuzione di RF sul tessuto biologico forma delle lesioni trans murali ed irreversibili; queste lesioni vengono generate per contatto termico (necrosi coagulativa) poiché la temperatura del tessuto biologico raggiunge 50/60 °C.
Nel caso di RF unipolare l’energia arriva fino alla punta del primo elettrodo ablatore, mentre il secondo elettrodo - di norma posizionato dietro la schiena del paziente – genera un’elevata energia a contatto con il tessuto biologico, che diminuirà man mano che l’elettrodo scenderà in profondità. Le alte temperature che si formano, possono causare delle carbonizzazioni del tessuto collegato con l’elettrodo ablatore e, questa carbonizzazione può impedire la realizzazione di una adeguata profondità della lesione. Per evitare questo possibile problema, sono stati creati elettrodi ablatori con punta irrigata, che mantengono temperature minori al contatto interfacciale elettrodo/tessuto.
LA MAPPATURA DELLE ARITMIE
La mappatura di una aritmia , ha la finalità di scoprire l’attività elettrica delle camere cardiache, raccogliere informazioni sull’ impulso elettrico, e la sua sequenza di attivazione.
Tutte queste informazioni permettono una mappatura ben precisa della camera cardiaca ,e dove andare eventualmente ad intervenire per escludere i trigger o il tessuto aritmogeno.
Uno dei primi sistemi di mappatura disponibili è stato il CARTO (BIOSENSE WEBSTER) STEREOTAXIS 2D, attualmente il CARTO 3D che usa un sistema a tre campi magnetici , e un microchip nella punta del catetere che viene manovrato dentro il cuore.
Tutto questo permette di creare un volume virtuale delle camere cardiache, più la registrazione dei segnali elettrici anomali.
Un ‘altro sistema di mappatura è l’ENSITE 3D (CARDIAC MAPPING) con sistema a reticolo di elettrodi, può definire una sequenza elettrica con un solo battito cardiaco.
IL sistema NAvX ( ENDOCARDIAC SOLUTION ), che utilizza tre campi elettrici a bassa tensione, a differenza del CARTO che utilizza un sistema a tre campi magnetici.
COMPLICANZE DELL’ABLAZIONE DELLA FIBRILLAZIONE ATRIALE.
- Stenosi delle vene polmonari.
- Trombo embolia.
- Fistola atrio esofagea.
- Flutter atriale sinistro.
- Embolia gassosa.
- Bradicardia.
- Tamponamento cardiaco.
- Paralisi nervo frenico.
EFFICACIA DELL?ABLAZIONE TRANSCATETERE DELLA FIBRILLAZIONE ATRIALE.
L’efficacia ablativa trans catetere a breve e medio termine, può variare per una serie di fattori legati al tipo di FA. Come scelta terapeutica e migliore nei soggetti con FA parossistica (60/70% dopo una singola procedura ) che nei pazienti con FA persistente o persistente di lunga durata (40/60% dopo una singola procedura ). La validità aumenta del (10/15%) dopo Multiple procedure (RITOCCO).
L’ablazione trans catetere della FA non può essere considerata una cura definitiva, ma un’opzione terapeutica,e con l’ausilio dei farmaci antiaritmici da utilizzare per un miglior controllo dell’aritmia e dei suoi sintomi.
Toni 2012
QRS LARGO ALL' ECG: SI TRATTA DI TACHICARDIA VENTRICOLARE O TACHICARDIA SOPRAVENTRICOLARE ?
Spesso, può capitare che osservando un tracciato ci si ponga questa domanda: di cosa si tratta? Siamo in presenza di una TACHICARDIA VENTRICOLARE o più semplicemente di una TACHICARDIA SOPRAVENTRICOLARE ?
Prima di tutto rispondiamo alla domanda più semplice: cos'è una tachicardia ? Risposta: si definisce TACHICARDIA quando la frequenza SUPERA I 100 BATTITI AL MINUTO.
In base alla durata si può distinguere se una tachicardia:
SOSTENUTA se dura PIU' di 30 secondi
NON SOSTENUTA se dura meno di 30 secondi
Una tachicardia può presentarsi:
a QRS STRETTI con un tempo di conduzione minore di 120 ms pari a meno di 3 millimetri di larghezza nella carta millimetrata oppure
a QRS LARGHI con un tempo di conduzione superiore o uguale ai 120 ms quindi uguale o superiore ai 3 millimetri di larghezza.
Le CAUSE che possono portare ad un QRS largo sono molteplicI,
Uno dei passi successivi è stabilire se la frequenza è regolare o non regolare.
Si definisce:
REGOLARE quando la distanza tra gli intervalli R-R quindi tra un battito e l'altro rimane COSTANTE, nella maggior parte dei casi se ci si trova il questa situazione la tachicardia sarà di origine VENTRICOLARE.
IRREGOLARE quando la distanza tra gli intervalli R-R VARIA.
Se la frequenza risulta REGOLARE, il QRS LARGO può dipendere da:
TACHICARDIA VENTRICOLARE IN CIRCA 80% DEI CASI
OGNI TACHICARDIA SOPRAVENTRICOLARE CONDOTTA CON BLOCCO DI BRANCA O ABERRANZA in cui i QRS APPAIONO LARGHI E DI MORFOLOGIA ovvero di forma DIVERSA DAL QRS SINUSALE.
OGNI TACHICARDIA SOPRAVENTRICOLARE A CONDUZIONE RITARDATA A CAUSA DI DISFUNZIONE ELETTROLITICA O DOVUTI ALL'ASSUNZIONE DI FARMACI ANTIARITMICI
TACHICARDIA DA WPW IN CUI l'impulso scende per una via ACCESSORIA e risale per la normale via di conduzione
TACHICARDIE CHE VENGONO CONDOTTE DAL PACEMAKER
Se la frequenza risulta IRREGOLARE, il QRS LARGO può dipendere da:
FIBRILLAZIONE ATRIALE CON BLOCCO DI BRANCA O ABERRANZA
OGNI TACHICARDIA SOPRAVENTRICOLARE CONDOTTA CON ABERRANZA PER LA PRESENZA DI UN BLOCCO DI BRANCA
I PRIMI 30 SECONDI DI TACHICARDIA VENTRICOLARE.:
I 5 CRITERI CHE RISOLVONO IL DILEMMA:
PRIMO CRITERIO: LA DURATA DEL QRS
Bisogna analizzare la derivazione precordiale V1, in caso di BLOCCO DI BRANCA SINISTRO se il QRS è maggiore di 160 ms ovvero più di 4 mm di larghezza alla carta millimetrata allora sicuramente si tratta di TACHICARDIA VENTRICOLARE, se inferiore bisognerà valutare la diagnosi,
In caso di BLOCCO DI BRANCA DESTRA analizzando sempre la derivazione precordiale V1 se il QRS è maggiore di 140 ms allora è indice di TACHICARDIA VENTRICOLARE mentre se è inferiore bisogna valutare la diagnosi
SECONDO CRITERIO: LA DISSOCIAZOPNE ATRIO VENTRICOLARE:
Questa condizione è indice sicuramente di TACHICARDIA VENTRICOLARE.
All'elettrocardiogramma appaiono più QRS che onde P poichè i ventricoli si attivano in numero maggiore rispetto agli atri
VARIETA' DI AMPIEZZA DEI QRS in cui uno o più complessi ventricolari appaiono diversi dagli altri
BATTITI DI CATTURA E DI FUSIONE in cui i QRS appaiono meno larghi ed è dovuto al fatto che l'impulso èroveniente dal nodo seno atriale attiva il nodo atrio ventricolare e parzialmente o interamente i ventricoli.
Se i ventricoli vengono attivati INTERAMENTE saranno presenti battiti di CATTURA
Se i ventricoli vengono attivati PARZIALMENTE saranno preenti battiti di FUSIONE..
TERZO CRITERIO: ASSE DEL QRS
Un asse elettrico ventricolare e quindi del QRS COMPRESO TRA -90° E I - 180° DEPONE ASSOLUTAMENTE PER UNA TACHICARDIA VENTRICOLARE
Così come una variazione dell'asse del QRS tra l'episodio aritmico e il ritmo sinusale è maggiore o uguale a 40° allora la diagnosi è suggestiva di TACHICARDIA VENTRICOLARE
QUARTO CRITERIO. CONCORDANZA DEL QRS
Si osservano tutte le DERIVAZIONI PRECORDIALI quindi da V1 A V6 se esse appaiono tutte con
QRS NEGATIVO la diagnosi è sempre di TACHICARDIA VENTRICOLARE
QRS POSITIVO la diagnosi è quasi sempre di TACHICARDIA VENTRICOLARE
QUINTO CRITERIO: COMPLESSI IN V1 E V6 E BLOCCO DI BRANCA DESTRA
Se guardiamo la derivazione precordiale V1 e ci accorgiamo che abbiamo un QRS A MORFOLOGIA rSr'' si tratta di una TACHICARDIA SOPRAVENTRICOLARE condotta con ABERRANZA
Se invece sempre in V1 abbiamo una R grande o una Rsr allora ci sarà diagnosi di TACHICARDUA VENTRICOLARE.
Se guardiamo la derivazione precordiale V6 e troviamo un complesso ventricolare RS allora si tratta di TACHICARDIA SOPRAVENTRICOLARE.
Se invece troviamo una R allora la diagnosi è di TACHICARDIA VENTRICOLARE.
Il quinto criterio prende in considerazione anche il QRS IN V1 E V6 E BLOCCO DI BRANCA SINISTRO
Se l'onda R in V1 è maggiore di 30 ms la diagnosi è di TACHICARDIA VENTRICOLARE
Se in V6 NON VI è PRESENZA DI ONDA q akkora la diagnosi depone per una TACHICARDIA SOPRAVENTRICOLARE CONDOTTA CON ABERRANZA
TACHICARDIE VENTRICOLARI (TV)
TACHICARDIE VENTRICOLARI (TV)
Le TV sono ritmi cardiaci con frequenze maggiori di 100 – 120 battiti per minuto (bpm), che originano nelle strutture ventricolari:
-nel sistema di conduzione cardiaco (miocardio specifico: si depolarizza spontaneamente, originando impulsi elettrici da trasmettere alle pareti muscolari dei ventricoli, i quali, in risposta alla stimolazione, normalmente si contraggono), distalmente al fascio di His;
-nelle pareti dei ventricoli (miocardio di lavoro, contrattile, che pompa il sangue nelle grandi arterie aorta e polmonare).
Nelle immagini seguenti, il miocardio specifico appare in colore giallo e quello di lavoro in colore carne. Tracciato ECG (elettrocardiografico) normale in basso e nella pagina successiva.



Le TV possono essere sostenute o non sostenute, a seconda della durata, maggiore (sicuramente sintomatiche) o minore (a volte asintomatiche) di 30 secondi.
Ancora, possono essere monomorfe, quando i complessi rapidi ventricolari o QRS – caratteristicamente slargati - sono tutti uguali, poiché originano da un unico focolaio e polimorfe quando essi variano da battito a battito, essendo generati da più focolai (situazione meno frequente, ma potenzialmente più sfavorevole).
Tre complessi QRS ventricolari anomali in sequenza configurano una TV.
L’immagine seguente esemplifica una traccia ECG di TV parossistica (= ad insorgenza improvvisa) monomorfa, con il particolare dell’unico focolaio di origine.

***********
I battiti ectopici ventricolari (BEV), o extrasistoli ventricolari (ESV), o complessi QRS ventricolari anomali, originati distalmente al fascio di His, che in numero di 3 in sequenza configurano una tachicardia ventricolare, costituiscono l’aritmia (= turba del normale ritmo sinusale cardiaco) ventricolare più comune e sono raffigurati nell’immagine seguente.

Sono ectopici perché originano al di fuori del nodo seno atriale del sistema di conduzione, unica sede fisiologica di origine degli impulsi elettrici cardiaci normali.
I BEV possono essere benigni, potenzialmente maligni o maligni, in relazione all’associazione, o meno, con cardiopatie strutturali più o meno severe.
Il TRATTAMENTO DEI BEV dipende dalla presenza o meno di significative cardiopatie strutturali sottostanti, quali, ad esempio, coronaropatie (soprattutto), disfunzioni ventricolari, cardiomiopatie (malattie del muscolo cardiaco), valvulopatie (malattie delle valvole cardiache).
In assenza di significative cardiopatie strutturali, i pazienti asintomatici non richiedono terapia, mentre i sintomatici possono essere utilmente rassicurati e/o trattati con ansiolitici, beta-bloccanti o calcio-antagonisti non diidropiridinici, quali verapamil o diltiazem, previa sospensione dei fattori aggravanti, quali caffeina, nicotina e alcool.
In presenza di cardiopatie strutturali, la gestione non può prescindere dal trattamento della cardiopatia stessa e da:
-mantenimento dell’equilibrio elettrolitico, soprattutto in relazione a Potassio e Magnesio;
-stretto controllo dell’ipertensione arteriosa (prevenzione dell’ipertrofia miocardica);
-farmacoterapia con antiaritmici;
-terapia ablativa, in caso di rifiuto o controindicazione alla farmacoterapia e in caso di BEV monomorfi (focolaio ectopico singolo);
-impianto di Pace Maker (PM) – Defibrillatore (ICD).
***********
Cause di TV
La TV si può sviluppare più facilmente come complicazione dell’infarto miocardico.
Può verificarsi anche in pazienti con:
- Cardiomiopatie (patologie del muscolo cardiaco) congenite o acquisite;
- Scompenso cardiaco;
- Pregressa cardiochirurgia;
- Miocardite (infiammazione del muscolo cardiaco, infettiva, autoimmune o chemio-radioindotta);
- Valvulopatie (malattie valvolari cardiache);
- Farmaci anti-aritmici (ad es. Digossina) o sostanze che aumentano l’eccitabilità del cuore (ormoni tiroidei, amfetamine, cocaina, ad esempio);
- Modifiche nella chimica del sangue (ad esempio bassi livelli di potassio, magnesio e calcio);
- Modifiche del pH ematico (squilibrio acido-base);
- Deficit di ossigenazione (patologie respiratorie, ad esempio);
- Contusioni cardiache traumatiche;
- Attività sportiva in cuori sani (brevissime salve isolate di 6 – 10 BEV consecutivi).
La sintomatologia delle TV può integrare:
-senso di testa vuota, ansia, agitazione, sincope (perdita di coscienza);
-tachipnea (incremento della frequenza respiratoria) e/o dispnea (difficoltà respiratoria);
-palpitazioni, dolore toracico, ipotensione (riduzione patologica della pressione sanguigna);
-arresto cardiaco (cardiopatie strutturali, soprattutto).
I sintomi possono avviarsi e interrompersi improvvisamente; in alcuni casi, nemmeno si avvertono, soprattutto nelle TV non sostenute.
Diagnosi: ECG (elettrocardiogramma), a riposo e/o durante sforzo:
Ecocardiogramma (anomalie cardiache strutturali);
Elettrocardiogramma continuo ambulatoriale (Holter);
Loop recorder (dispositivo impiantabile sottocute di piccole dimensioni che controlla costantemente il ritmo cardiaco e lo memorizza in modo automatico o manuale);
Studio di elettrofisiologia intracardiaca (EPS);
Esami ematochimici: emocromo, glicemia, elettroliti, creatinina, troponine, TSH, FT3, FT4, ricerca di sostanze cardiotossiche (amfetamine e cocaina, ad esempio).
Trattamento: dipende dalle condizioni del paziente.
Il paziente in arresto cardiaco o instabile (sintomi avversi come sincope, difficoltà respiratorie, dolore toracico, ipotensione o frequenze cardiache > 150 battiti per minuto) va prontamente e urgentemente trattato, per il ristabilimento del ritmo sinusale, possibilmente:
-defibrillazione, mediante shock elettrico, in caso di arresto cardiaco da ritmi defibrillabili, quali tachicardia ventricolare senza polso (in assenza di circolo) e fibrillazione ventricolare;
-cardioversione elettrica, negli altri casi.
Il paziente stabile, paucisintomatico, potrà essere osservato ed eventualmente trattato farmacologicamente con antiaritmici o elettricamente.
La terapia a lungo termine prevede:
-norme igieniche: abolizione di caffè, tabacco, alcool ed eventuali sostanze di abuso; dieta iposodica, normo-ipocalorica, di tipo mediterraneo; attività fisica non eccessiva;
-farmaci anti-ipertensivi, se indicati, tra cui antialdosteronici o ACE-inibitori;
-controllo lipidemico (colesterolo), eventualmente farmacologico (statine) ed elettrolitico (magnesio e potassio);
-farmaci antiaritmici; farmaci normalizzanti la funzione tiroidea;
-ablazione percutanea (mediante catetere intravascolare a radiofrequenza) per via endocardica (attraverso la superficie interna del cuore) o epicardica (puntura sub-xifoidea, in caso di insuccesso del cateterismo cardiaco), attraverso la superficie esterna del cuore, soprattutto in assenza di cardiopatie strutturali significative;
-posizionamento sottocutaneo di Pace Maker (PM) -Defibrillatore (ICD), impiantabile per via percutaneo-venosa, come un normale PM, in grado di interrompere i BEV e le TV, soprattutto in caso di cardiopatie strutturali;
-trattamento delle cardiopatie strutturali sottostanti.
Di seguito, uno schema riportante la classificazione dei farmaci antiaritmici.

L’immagine successiva riporta l’esemplificazione di un cateterismo cardiaco, con cui eseguire studi elettrofisiologici e ablazioni.

Esempio di accesso percutaneo epicardico.

Nell’immagine seguente, un Loop-reconder posizionato sottocute.

Nell’immagine successiva, un ICD posizionato sottocute e connesso alle camere cardiache.

A seguire, l’algoritmo internazionale di trattamento dell’arresto cardiaco, più spesso cagionato da aritmie ventricolari maligne, quali tachicardia ventricolare senza polso e fibrillazione ventricolare.
Legenda:
ALS = Advanced life Support = Supporto Vitale Avanzato
RCP = Rianimazione Cardio-Polmonare
FV = Fibrillazione Ventricolare
TVSP = Tachicardia Ventricolare Senza Polso
(FV e TVSP = ritmi più frequenti dell’Arresto Cardio-Circolatorio [= ACC] e defibrillabili)
PEA = Pulseless Electrical Activity = Attività Elettrica (qualunque ritmo, non FV o TVSP) senza polso (cioè non capace di produrre circolazione valida, ovvero palpabile), situazione in passato nota come DEM = Dissociazione Elettro-Meccanica.
Asistolia (ASY) = assenza di attività elettrica cardiaca.
(PEA e ASY = ritmi meno frequenti dell’ACC e NON defibrillabili).
Di seguito, la raffigurazione dell’elettroterapia antiaritmica (cardioversione/defibrillazione).

L’immagine successiva illustra il funzionamento di un defibrillatore semiautomatico, in grado di rilevare i ritmi cardiaci patologici e guidare il soccorritore nell’erogazione dello shock elettrico, ove necessario.


Lo schema soprastante costituisce un esempio di algoritmo terapeutico per la cardiopatia ischemica, causa comune di aritmie ventricolari.
Si specifica che, in caso di dolore toracico, le seguenti condizioni sono da considerare, in ordine di frequenza:
-patologie gastroenteriche (reflusso gastroesofageo, malattia peptica, calcoli biliari): 40%;
-cardiopatia ischemica: 30%;
-algie di parete della gabbia toracica (muscoli, ossa, cartilagini): 25%;
-altre (pericardite, pleuropolmonite, embolia polmonare, tumore polmonare, aneurisma aortico, stenosi aortica, herpes zoster o fuoco di Sant’Antonio): 5%.
In conclusione e al fine di esemplificare la gravità delle TV, si propone il seguente schema riassuntivo e classificativo:
- TV che non compromettono la circolazione sanguigna, con disturbi minori (palpitazioni, sensazione di testa vuota, ansia, ad es.) o del tutto asintomatiche, richiedentiosservazione, rassicurazione ed eventuali trattamenti sintomatici e a lungo termine, in relazione alla eventuale presenza di cardiopatie strutturali associate;
- TV che compromettono la circolazione sanguigna, senza causare ACC, ma che provocano sintomi avversi (turbe della coscienza, difficoltà respiratorie, dolore toracico, ipotensione arteriosa, frequenza cardiaca > 150 bpm) che richiedono trattamenti immediati e a lungo termine;
- FV/TVSP, cause più frequenti di ACC e Morte Cardiaca Improvvisa: il cuore è fermo e cessa di pompare sangue agli organi, soprattutto al cervello (→ perdita di coscienza e conseguente arresto respiratorio immediati). L’assenza di circolazione (incompatibile con la vita) impedisce l’apprezzamento di pulsazioni arteriose (polsi carotidei assenti e dunque impalpabili). Richiedono immediata RCP e attivazione della catena di emergenza/soccorso (118, per il territorio), essendo la sopravvivenza del paziente strettamente dipendente dalla celerità d’intervento, volto al ripristino della circolazione sanguigna spontanea (ROSC = Return Of Spontaneous Circulation), attraverso il recupero di un ritmo cardiaco con esso compatibile.
L’immagine seguente illustra la catena di sopravvivenza.
BIBLIOGRAFIA
Antonelli, “Extrasistolia Ventricolare Benigna”, Cardiology Science, 2010.
Chung, “Ventricular Tachycardia”, Netter’s Cardiology II ed., Saunders – Elsevier Edit.
Compton, “Ventricular Tachycardia”, Medscape, 2014.
Dave, “Ventricular Premature Complexes”, Medscape, 2014.
Dubin, “Rapida Interpretazione Dell’ECG”.
Fauci, “Harrison’sPrinciples Of Internal Medicine”, Mc Graw Hill, 2012.
Merck Manuale online, “Tachicardie Ventricolari”.
Romano, “Il Malato Critico”, UTET, 2000.
SINDROME DI BRUGADA - CHI HA RAGIONE ?????
Pubblicato il: 22/09/2015
Scacco italiano alla morte improvvisa, guarita la sindrome di Brugada
Successo italiano senza precedenti al mondo nella lotta alle aritmie cardiache maligne responsabili della morte improvvisa, un fulmine a ciel sereno che solo nel nostro Paese uccide almeno 50 mila persone all'anno. Vite stroncate sul nascere, a volte sotto i riflettori di una partita di calciocome è capitato al centrocampista Piermario Morosini, 25 anni, crollato in campo il 14 aprile 2012 al 31esimo minuto di Pescara-Livorno. Displasia aritmogena del ventricolo destro il nome del killer inchiodato dall'autopsia, una patologia genetica 'cugina' della Sindrome di Brugada che oggi trova alle porte di Milano una cura definitiva. Venticinque pazienti guariti, liberati per sempre dall'angoscia di svegliarsi ogni giorno sapendo di portare nel petto una bomba a orologeria. Vivono così oltre mezzo milione di connazionali, molti dei quali malati senza saperlo.
L'autore della scoperta destinata a entrare nella storia della medicina si chiama Carlo Pappone, nome ben noto alla comunità aritmologica mondiale: in curriculum 150 mila cuori operati, 295 pubblicazioni, 12 mila citazioni, impact factor superiore a 1.200. Beneventano, classe 1961, dal 1 marzo dirige l'Unità operativa di Elettrofisiologia e Aritmologia dell'Irccs Policlinico San Donato, inaugurata alla presenza del governatore della Regione Lombardia Roberto Maroni e del cardiologo spagnolo Josep Brugada. Nel 1992 è stato lui, insieme al fratello Pedro, a fornire sul 'Journal of American College of Cardiology' la descrizione più completa della sindrome che porta il cognome di famiglia e causa il 15-20% delle morti improvvise fra gli under 40.
E ora è proprio Brugada a firmare insieme a Pappone l'articolo della svolta, che apparirà in ottobre su 'Circulation EP' dopo un'anticipazione pubblicata in agosto sulla versione online della rivista. Una tecnica di ablazione 'al bersaglio', che con una corrente elettrica a radiofrequenza brucia selettivamente le cellule cardiache responsabili della patologia genetica ereditaria, dopo averle individuate attraverso un mappaggio elettromagnetico del ventricolo destro. Quattordici i pazienti protagonisti dello studio, maschi come praticamente tutti i malati di Brugada, età media 39 anni, già portatori di un defibrillatore impiantabile. Dal giorno dell'intervento (il primo è stato eseguito lo scorso novembre) hanno l'elettrocardiogramma normale e nessun segno clinico di malattia, e possono sperare nell'espianto del defibrillatore. I medici lo ritengono fattibile "dopo un anno senza sintomi e con Ecg normale".
Per gli esperti non si può che chiamarla "rivoluzione". La notizia, afferma Pappone, "sarà molto importante per tutti quei pazienti che, consapevoli di avere la Sindrome di Brugada, vivono nel terrore delle conseguenze della loro malattia. Altri tentativi per eliminarne i sintomi, e in particolare le aritmie, erano stati eseguiti nel passato con buona percentuale di successo. Ma non avevano come obiettivo l'eliminazione completa della malattia. Questo - precisa l''elettricista del cuore' - è il primo studio al mondo in cui una malattia genetica può scomparire applicando una speciale corrente elettrica attraverso un sondino che raggiunge la superficie del ventricolo destro".
L'intervento è in anestesia generale e prevede un ricovero di 3-4 giorni. "Con un ago, pungendo la parte inferiore dello sterno - spiega Pappone - introduciamo un sondino che viene spinto fino a raggiungere la superficie esterna del cuore (l'epicardio) e ne rileva i segnali elettrici. In questo modo ricostruiamo l'anatomia e l'attività elettrica dell'organo, individuando con precisione il punto esatto del ventricolo destro in cui si esprime la malattia. Quella è la zona da bruciare" e a seconda dei casi può essere più o meno estesa: "Da alcuni centimetri quadrati a molti, fino ad arrivare a un terzo dell'intero ventricolo. In base all'estensione della patologia potranno quindi essere necessarie da 5 a 30 applicazioni di energia a radiofrequenza. Nelle forme più aggressive, poi, oltre alla Brugada possiamo trovare una displasia del ventricolo destro. Nel 15% dei pazienti le 2 condizioni coesistono e si potenziano l'una con l'altra, aumentando ulteriormente il rischio di morte improvvisa".
Dei 25 guariti (dopo i 14 casi pubblicati gli interventi sono proseguiti), 8 sono stati operati nel Ravennate al Maria Cecilia Hospital di Cotignola, dove Pappone ha lavorato prima di arrivare a San Donato Milanese e dopo gli anni trascorsi all'Irccs San Raffaele di Milano. Gli altri 17 sono stati curati al Policlinico San Donato dove tutta l'équipe del medico si è trasferita. "La tecnica che abbiamo messo a punto - puntualizza l'ideatore - richiede mezzi (l'intervento costa all'ospedale circa 10 mila euro a fronte di un rimborso regionale-Drg di 6 mila, quindi vuol dire che per ogni procedura perdiamo 4-5 mila euro), ma soprattutto esperienza e competenza. La nostra intenzione, dunque, è quella di creare un centro di eccellenza per la diagnosi e la cura della Sindrome di Brugada. Un polo per attrarre pazienti da tutto il mondo".
I numeri non sono piccoli. "In Europa la Sindrome di Brugada ha una diffusione relativa - riferisce Pappone - e in Italia si stima nascano da 0,4 a 1,7 bimbi malati ogni 10 mila, con una prevalenza dello 0,7-2,5%. Ma questo dato sale al 6% in Francia, all'11% nelle nazioni del Medio Oriente e al 12% in Thailandia".
I 'bambini Brugada' vengono alla luce con dentro "un orologio che indica l'ora in cui il loro cuore un giorno si fermerà, e la grande sfida è identificarli prima che accada. Dei pazienti italiani, uno su 3 è ad alto rischio di morte improvvisa e un terzo di questi non sa di avere la patologia. O perché non ha mai fatto un Ecg, o perché inizialmente nel tracciato l'alterazione non compariva. Oppure perché la prima manifestazione clinica della malattia è stata la morte per arresto cardiaco". Una verità scoperta troppo tardi, magari da una scritta sull'autopsia
"In genere - continua lo specialista - questi pazienti muoiono in concomitanza con una febbre alta, una malattia infettiva o un''overdose' alimentare. La malattia è scritta nel Dna e in particolare è legata al sesso maschile. Tanto che in alcuni Paesi del mondo, ad esempio in Thailandia o nelle Filippine, quando in una famiglia segnata da altri casi di morte improvvisa viene alla luce un maschietto lo vestono da femmina". Un disperato tentativo di 'depistare' la sorte, di sfuggire a quella che si considera "una maledizione, una malattia oscura. La Brugada è infatti una patologia autosomica dominante, il che vuol dire che se il padre ce l'ha anche il figlio ha il 50% di probabilità di soffrirne".
"Oggi siamo in grado di identificare solo un gene responsabile, positivo nel 25% pazienti - prosegue Pappone - ma resta scoperto l'altro 75% e l'ipotesi è che siano coinvolti tanti punti del Dna. In molti casi alla Brugada si associano altre patologie come displasie aritmogene o sindromi del QT lungo e corto", con un effetto moltiplicativo sul pericolo di morte improvvisa.
"Finora - ricorda ancora l'esperto - l'unica terapia possibile per i pazienti con una diagnosi era l'impianto di un defibrillatore, una sorta di pacemaker che eroga la sua scarica quando il cuore si ferma". Non una cura bensì un palliativo, il tentativo di prevenire l'irreparabile. "Oggi nel mondo vivono molte migliaia di uomini portatori di un defibrillatore impiantabile perché affetti da Sindrome di Brugada ad alto rischio di morte improvvisa". Per questi, e per l'esercito di malati che ancora devono scoprire di esserlo, è da oggi disponibile la prima vera cura. "L'unica che ha dimostrato di eliminare la patologia" fulminandola al cuore.
Il gol è frutto di un 'assist' Italia-Spagna, la cui traiettoria incrocia anche i Caraibi. "Era un giorno di giugno del 2014 e mi trovavo a Cuba - racconta l''uomo dei 150 mila cuori' - A nche Josep (Brugada, ndr) stava provando a entrare nel Paese dagli Usa, ma ha avuto un problema con il visto. Quando gli hanno riferito che mi trovavo lì mi ha telefonato e la sua chiamata mi ha raggiunto mentre avevo di fianco il ministro degli Interni. Pochi minuti dopo Josep passava la frontiera. Allora gli ho detto che avevo un'idea per guarire la 'sua' sindrome, e che il modo migliore per ringraziarmi sarebbe stato quello di farmi provare. Lui era scettico, ma in ottobre è venuto a Cotignola e ha dovuto ricredersi".
"Ci hanno detto 'è impossibile, non funzionerà mai'. Ma abbiamo lavorato duro e ora, 25 anni più tardi, possiamo dire che con il trattamento messo a punto da Carlo Pappone cambia la storia naturale di una malattia devastante. Devastante per i malati e per le famiglie soprattutto dei pazienti più giovani". E' lo stesso Josep Brugada a parlare di "pietra miliare" e di "svolta" per descrivere il risultato ottenuto con la nuova metodica. Ora, assicura,"questo centro di eccellenza può diventare capofila di un network internazionale che attrarrà pazienti con la sindrome di Brugada da tutto il mondo. Nei loro cuori si potranno eliminare le conseguenze di questa malattia genetica ed è incredibile. Abbiamo messo insieme - spiega - l'esperienza di Pappone nel campo dell'ablazione, che è la numero uno al mondo, con la nostra conoscenza della malattia sul fronte genetico e siamo stati capaci di imprimere una svolta".
"Tutti ci siamo emozionati e abbiamo sentito battere il nostro cuore all'impazzata almeno una volta nella vita - dice Pappone - Ecco, l'aritmia è una malattia misteriosa che non si vede, non si palpa. Il sogno sono diagnosi certe e terapie possibili". Al San Donato, nel nuovo reparto "l'attività è stata organizzata anche come numero di posti letto per poter fare circa 3.500 interventi all'anno - prosegue lo specialista - Adesso applicheremo la tecnica che ci ha permesso di curare la sindrome di Brugada sia su pazienti italiani sia su pazienti che vengono da altri Paesi: da tutto il mondo saranno inviati qui. E poi il passo successivo sarà di insegnare ai medici anche stranieri come eseguire questa procedura. Partirà uno studio a breve".
E "anche se è tutto ancora nuovo, speriamo di poter convincere gli amministratori a modificare la tariffa del Drg perché oggi viene rimborsata circa la metà del costo della procedura", conclude Pappone. "Abbiamo intenzione di fare quello che serve", dichiara il governatore lombardo Roberto Maroni a margine dell'inaugurazione, precisando che "le risorse sono quello che sono, ma la prospettiva è di aumentarle. Tutto passa dai costi standard: se diventano realtà questi problemi si superano. Altrimenti la coperta rimarrà corta e dovremo decidere dove mettere le risorse".
RISPOSTA :
Pubblicato il: 24/09/2015
Pedro Brugada attacca studio sulla morte improvvisa: "Dà false speranze"
Pedro Brugada, che insieme al fratello Josep ha descritto nel 1992 l'omonima sindrome responsabile del 15-20% dei casi di morte improvvisa tra gli under 40, attacca in una lettera l'annuncio di una cura definitiva contro la malattia, diffuso dopo la pubblicazione di uno studio co-firmato dallo stesso Josep Brugada e da Carlo Pappone, direttore dell'Unità operativa di Elettrofisiologia e Aritmologia dell'Irccs Policlinico San Donato Milanese.
Un colpo a sopresa con Pedro che rivolge "alcune critiche importanti", si legge nella missiva ricevuta dall'AdnKronos Salute, "a causa delle aspettative sbagliate" che la notizia "ha creato tra i miei pazienti, spinti dalla vana speranza di poter definitivamente 'guarire'" dalla patologia.
Dopo l'annuncio del 22 settembre "il nostro centro è stato ripetutamente contattato da pazienti per chiarimenti", scrive Pedro Brugada, direttore del Cardiovascular Center e dell'Heart Rhythm Management Center dell'Universitair Ziekenhuis di Bruxelles. L'esperto premette di conoscere "il dottor Pappone da tempo: è una delle menti più creative nel settore dei disturbi del ritmo del cuore, e un potenziale modello da seguire per futuri cardiologi. Tuttavia - precisa - la commercializzazione della medicina non deve sopraffare la realtà scientifica".
La tecnica descritta da Pappone e Josep Brugada su 'Circulation EP' (il lavoro è uscito online in agosto e comparirà in ottobre sulla versione cartacea della rivista), afferma Pedro Brugada, "in realtà è già stata descritta dal collega Koonlawee Nademanee (che lavora presso l'università della California) in una pubblicazione riguardo a questo trattamento circa 4 anni fa. Non c'è nulla di nuovo: Nademanee aveva già dimostrato tutto", sostiene lo specialista citando il titolo del lavoro uscito nel 2011 su 'Circulation'. "Il punto principale al quale voglio arrivare - puntualizza - non si riferisce al trattamento stesso, già peraltro dimostratosi efficace come si può intuire leggendo l'articolo di Nademanee, ma a chi dovrebbe essere rivolto questo trattamento, e se questo può essere una valida alternativa all'impianto del defibrillatore (Icd)".
"Con migliaia di pazienti con sindrome di Brugada in tutto il mondo trattati con un Icd - osserva Pedro Brugada - nessuna pubblicazione ha messo in discussione il valore positivo di questa terapia per prevenire la morte cardiaca improvvisa. I pazienti con la sindrome in questione sono giovani (età media 40 anni) e possono avere una vita tranquilla, nonostante l'impianto di un Icd. In realtà, non sono poste limitazioni per quanto riguarda lo sport o altre attività, in quanto sono costantemente protetti dall'Icd".
"Il trattamento ablativo descritto da Pappone" su 14 malati di Brugada portatori di Icd (dopo la pubblicazione di agosto gli interventi sono saliti a 25), secondo Pedro Brugada "ha come solo obiettivo quello di trattare quella porzione di pazienti affetti dalla sindrome che subiscono ripetuti 'shock' terapeutici erogati dal defibrillatore per l'interruzione di aritmie ventricolari maligne. Pertanto l'ablazione può trattare in casi estremi queste aritmie, ma di certo non 'guarisce' una malattia genetica come la sindrome di Brugada. Il paziente dovrà comunque subire un impianto di Icd per proteggersi dalla morte improvvisa", afferma l'esperto.
"Dal nostro centro di Bruxelles (UZ-Brussel-VUB), insieme ai professori Gian-Battista Chierchia e Carlo de Asmundis - conclude Pedro Brugada - non abbiamo inviato alcun comunicato stampa con false speranze, anche dopo aver eseguito numerose ablazioni con successo in pazienti affetti dalla sindrome di Brugada e da aritmie ventricolari ricorrenti. Abbiamo pubblicato i nostri dati sulla crioablazione della fibrillazione atriale in pazienti con sindrome di Brugada su importanti riviste scientifiche, ma non siamo mai andati alla stampa per promuovere l'ammissione di pazienti nel nostro centro o per incrementare il Drg per il rimborso della procedura".
"La nostra non deve apparire come la diffusione di una illusione - replica Pappone all'AdnKronos Salute - ma come una grande speranza per tanti pazienti che vivono nel terrore della prossima scarica del defibrillatore o delle complicanze dello stesso legate a infezioni o malfunzionamenti, così come già pubblicato su 'Jacc' dal gruppo del professor Pedro Brugada", assicura l'esperto auspicando "che tale lettera scritta da Pedro Brugada, eminente ricercatore in questo campo, non nasconda una certa animosità familiare". Pappone spiega che "quanto riferito da me, insieme al professor Josep Brugada, risponde esattamente a ciò che è stato recentemente pubblicato su 'Circulation: Arrhythmia and Electrophysiology'".
Nell'articolo "si documenta la scomparsa della malattia in 14 pazienti e la conferma di tale risultato dopo 6 mesi di follow-up", e "non si fa riferimento alcuno alla suddetta inadeguatezza del defibrillatore", puntualizza il noto aritmologo, all'attivo 150 mila cuori operati. Nelle comunicazioni rilasciate alla stampa, "semplicemente, si dice che il defibrillatore è un palliativo e non rappresenta una cura definitiva, come il professor Pedro Brugada sa benissimo". Sia nelle interviste che nell'articolo, evidenzia ancora Pappone, si fa già "riferimento alla prima pubblicazione del dottor Nademanee, il quale con successo ha ottenuto l'abolizione delle aritmie ventricolari in circa il 60% di 9 pazienti".
"Nell'articolo - prosegue lo specialista - è ben chiaro che la tecnica ha come obiettivo non solo l'eliminazione delle aritmie, ma anche l'abolizione completa del pattern elettrocardiografico e quindi della malattia. La differenza è sostanziale poiché l'elettrocardiogramma di tutti i pazienti è diventato e stabilmente rimasto normale nel tempo, dopo l'intervento. I pazienti non hanno presentato più la malattia e non hanno più avuto aritmie ventricolari".
"Tutti i pazienti sottoposti all'intervento erano portatori di defibrillatore e quest'ultimo non è stato espiantato a nessuno", ricorda Pappone. "Non escludiamo che nel prossimo futuro, se i risultati fossero confermati nel lungo termine, questa strategia rappresenti un'ipotesi plausibile. Venendo cosi meno i motivi per l'impianto del defibrillatore, non essendovi più evidenza di malattia, è possibile che l'ablazione diventi non solo complemento, ma alternativa al defibrillatore. Quindi se il risultato persisterà nel corso degli anni - dice - il defibrillatore potrà persino essere espiantato o non sostituito quando la batteria sarà scarica".
"Per quanto concerne l'illazione che tale notizia sia stata diffusa per interessi personali o economici - incalza l'esperto - si fa presente che tale intervento è rimborsato solo per la metà dei suoi costi e rappresenta una perdita economica per l'ospedale. Il nostro lavoro è fatto di passione, di curiosità per la conoscenza al servizio del bene dei pazienti".
Infine, "per quanto riguarda il riferimento del professor Pedro Brugada a suoi interventi eseguiti su pazienti affetti da sindrome di Brugada, risulta che sia semplicemente un intervento diretto alla cura delle aritmie ventricolari, come del resto aveva già fatto Nademanee. Nessuno dei suoi pazienti è guarito dalla sindrome di Brugada, ma soltanto dalle aritmie". Pappone conclude con "il collegamento all'articolo in questione che conferma le nostre affermazioni".
La scelta degli anticoagulanti che proteggono dall’ictus e dall’embolia polmonare
Prevenire l’ictus da fibrillazione atriale e l’embolia polmonare da trombosi venosa delle gambe (fibrillazione atriale e trombosi venosa portano alla formazioni di coaguli di sangue che poi arrivano al cervello o ai polmoni, provocando danni anche mortali) è un imperativo della pratica clinica, ma che farmaci usare?
I vecchi anticoagulanti che inibiscono la vitamina K e impediscono la formazione di trombi (il classico warfarin) o i nuovi Noacs, anticorpi monoclonali (ce ne sono tre sul mercato e uno in arrivo) che fanno lo stesso mestiere, anzi sono anche più efficaci, ma ancora non vengono ben accettati da medici e pazienti per il rischio di emorragie? Se lo domanda un editoriale del New England e se lo sono domandati gli specialisti a Londra in occasione dell’Esc, il congresso della società europea di cardiologia.
«I nuovi anticoagulanti sono efficaci e sicuri — commenta Riccardo Cappato, direttore del Centro di Ricerca delle aritmie cardiache all’Istituto Humanitas di Milano) — e sono superiori nel prevenire ictus e embolie polmonari rispetto al warfarin. In più: non richiedono controlli della coagulazione, non interagiscono con i cibi e nemmeno con altri farmaci come il warfarin».
Tanto per dare un numero: gli inibitori della vitamina K riducono del 66 per cento il rischio di ictus nei pazienti con fibrillazione atriale, i nuovi anticoagulanti dell’ 80 per cento.
«I quattro nuovi farmaci (rivaroxaban, apixaban e edoxaban), che inibiscono il fattore Xa della coagulazione, e il dabigatran che inibisce la trombina — precisa Cappato — funzionano nel prevenire non solo ictus da fibrillazione atriale, ma anche embolie polmonari da trombosi venosa cronica delle gambe e il rischio di embolie in chi, per esempio, è immobilizzato dopo una frattura ossea o un intervento chirurgico».
«L’eparina per puntura sottocutanea non è più necessaria — commenta Cappato —. La possono sostituire i nuovi anticoagulanti somministrabili per bocca. Per certi versi questi sono trattamenti rivoluzionari».
Rimane il problema degli effetti collaterali, primo su tutti il rischio di emorragia. Se per il warfarin esistono antidoti specifici, per i nuovi anticoagulanti no (anche se si stanno studiando) si può soltanto ricorrere a terapie standard (come la somministrazioni di fluidi o di plasma sanguigno). Comunque i dati della ricerca rassicurano. «Lo studio Xantus, il primo condotto nel “mondo reale” (ha valutato cioè le terapie prescritte dai medici al di fuori da sperimentazioni) e pubblicato sull’European Heart Journal — ha confermato John Camm, cardiologo alla St George’s University di Londra — ha dimostrato che i rischi di sanguinamento legati alla somministrazione del rivaroxaban sono inferiori a quelli del warfarin, a parità di efficacia».
Corriere della Sera 20/09/2015
A. Bz.
Riproduzione riservata
Il defibrillatore chiama il medico Cumis
«La novità del dispositivo è che il paziente può effettuare la Risonanza»
Un defibrillatore per la resincronizzazione cardiaca, compatibile con la risonanza magnetica, è stato impiantato su un paziente affetto da scompenso cardiaco «refrattario alla terapia farmacologica». L'intervento, che rappresenta una novità nella terapia per lo scompenso, è stato effettuato da Antonio Curnis, responsabile laboratorio elettrofisiologia del Dipartimento di Cardiologia dell'Ospedale Civile di Brescia, sede di Cattedra universitaria, diretto dal prof. Livio Dei Cas.
«Un risultato importante, perché permette di migliorare la qualità di vita ad un numero crescente di persone - spiega Curnis -. Solo in Italia, infatti, il 2% della popolazione è affetta da scompenso cardiaco e la percentuale aumenta dopo i settant'anni. Molti pazienti non hanno benefici dalla terapia farmacologica convenzionalmente seguita per la loro patologia ed hanno bisogno di stimolatori elettrici impiantabili che siano in grado di resincronizzare l'attività cardiaca, migliorandone la contrazione e la funzione di pompa attraverso la stimolazione del cuore».
Brescia, da oltre un decennio, vanta risultati importanti nello sviluppo di questa terapia. «Del resto, lo scompenso cardiaco è una malattia complessa, perché il paziente non ha solo un deficit cardiaco - continua Curnis -. A questa patologia, infatti, ne sono correlate molte altre: problemi ai reni, ai polmoni, di pressione arteriosa e con aritmie. Il trattamento non si limita all'impianto del dispositivo, ma ad un costante controllo diagnostico in grado di limitare il numero dei ricoveri e anche, nella peggiore delle ipotesi, il tasso di mortalità». Quale il beneficio dell'intervento eseguito dal dottor Curnis e dalla sua équipe? «Tutti i pazienti impiantati finora non possono eseguire la Risonanza magnetica, uno dei più efficaci ed affidabili strumenti diagnostici. Questo perché, dopo l'impianto, la presenza dei cateteri e del dispositivo è causa di impedimento: il rischio che il campo magnetico induca un riscaldamento elevato della punta dei cateteri, o una impropria attivazione dei dispositivi, fa sì che ad oggi la normativa proibisca tale metodo diagnostico per tutte le persone portatici di stimolatori cardiaci, siano essi pacemaker o defibrillatori. Questo, malgrado la stima indichi in sette persone su dieci il numero di coloro che potrebbe aver bisogno di una Risonanza magnetica pur avendo uno stimolatore cardiaco». La novità nella tecnologia medica consiste nella realizzazione di pacemaker di altissima specializzazione compatibili con la Risonanza. Non solo. «I nuovi defibrillatori trasmettono ogni giorno, attraverso un telefono cellulare dedicato consegnato al paziente alla dimissione, tutti i dati tecnici e clinici del dispositivo: questo permette di controllare il paziente ogni giorno e di prevenire eventi clinici importanti - conclude Curnis -. E, in una fase di restrizioni economiche per tutti, si riducono anche le visite ambulatoriali con beneficio sia per la qualità della vita del paziente sia per i conti del Servizio sanitario».
Questo indirizzo email è protetto dagli spambots. È necessario abilitare JavaScript per vederlo.
riproduzione riservata © www.giornaledibrescia.it
TRATTAMENTO CHIRURGICO E TORACOSCOPICO IBRIDO DELLA FIBRILLAZIONE ATRIALE
Nel mese di Marzo si è svolto a Varese presso l'ospedale di Circolo e fondazione Macchi un congresso dal titolo TRATTAMENTO CHIRURGICO E TORACOSCOPICO IBRIDO DELLA FIBRILLAZIONE ATRIALE nel quale erano presenti il Prof. Cesare Beghi direttore della cardiochirurgia dell'ospedale di Circolo, il Prof Roberto De Ponti Professore associato di Cardiologia università degli studi dell'Insubria, il Prof. Antonio Curnis responsanile di aritmologia dell'ospedale civile di Brescia e il Prof. Muneretto responsabile della cardiochirurgia di Brescia.
All'inizio del congresso oltre alla classica suddivisione dei vari tipi di fibrillazione atriale come sappiamo già tutti in PAROSSISTICA, PERSISTENTE E PERMANENTE si è data importanza al fatto di come la fibrillazione atriale non sia più solo una patologia prevalentemente presente in una popolazione anziana, ma si sta sviluppando sempre più frequentemente anche nei quarantenni che cresce esponenzialmente con l'avanzare dell'età poichè il cuore invecchia e conseguentemente si ha un rimdellamento atriale per decrescere verso i novantanni
Si è visto come nella FIBRILLAZIONE ATRIALE PAROSSISTICA ovvero di breve durata e che tende al ripristino del ritmo sinusale spontaneamente, le responsabili dell'insorgenza di questa aritmia siano le VENE POLMONARI sia SUPERIORE DESTRA CHE SUPERIORE SINISTRA raramente sono quelle inferiori mentre nella FIBRILLAZIONE PERSISTENTE E PERMANENTE ciò che innesca tale aritmia sia il SUBSTRATO ATRIALE che porta ad un rimodellamento e ingrandimento degli atri.
La cardioversione farmacologica prima e la cardioversione elettrica sono le teraie di prima scelta nel ripristino del ritmo sinusale mentre i farmaci antiaritmici, AMIODARONE come farmaco di prima scelta viene utilizzato come terapia nel mantenere il ritmo sinusale.
Se nonostante i farmaci antiaritmici vi fossero delle recidive di fibrillazione atriale ecco che allora l'ablazione transcatetere sembra essere l'unica scelta da provare in prima istanza. DOMANDA::vi siete mai chiesti perchè dopo alcuni giorni dopo l'ablazione transcatetere endocavitaria possono manifestarsi recidive di fibrillazione atriale nonostante che durante terapia ablativa non si siano sviluppati potenziali da poter far pensare all'innesco di fibrillazione atriale ? Le risposte possono essere due: la formazione di edema nella zona ablata oppure il fatto che nel substrato esterno dell'atrio ovvero il PERICARDIO possono essere presenti deI FOCUS ECTOPICI che sviluppano potenziali tali da poter innescare fibrillazione atriale.
Quindi allora che si fa? In entrambi i casi ci sono le risposte: Nel primo caso se si sospetta la presenza di edema si lascia che esso venga riassorbito e se poi si manifesta ancora recidive di fibrillazione atriale si procede ancora all'ablazione andando a bloccare i potenziali attivi. Nel caso in cui non ci fosse formazione di edema ma le recidive di fibrillazione atriale parossistica fossero numerose il sospetto che ci siano foci esterne in grado di attivare l'innesco di fibrillazione atriale nel substrato è un'ipotesi ben documentato.
Da qui l'idea di una collaborazione tra ELETRROFISIOLOGO ( il professor CURNIS ) E CARDIOCHIRURGO (il professor MUNERETTO ) agli spedali di Brescia, Insieme hanno sviluppato un trattamento chirurgico e toracoscopico ibrido della FA. Vi domanderete, perchè IBRIDO ? Risposta: Perchè unisce nello stesso intervento sia un'ABLAZIONE ENDOCAVITARIA effettuata dall' ELETTROFISIOLOGO sia un'ABLAZIONE PERICARDICA effettuata dal CARDIOCHIRURGO IN TORACOSCOPIA.
Questa opzione per il trattamento della fibrillazione atriale può essere effettuato sia per la fibrillazione atriale parossistica in cui le recidive siano davvero numerose sia per le fibrillazioni atriali persistenti e permanenti quando nonostante la terza o quarta ablazione tradizionale sia fallita e può essere una valida alternativa alla MAZE III E IV.
Per la fibrillazione Triale PAROSSISTICA Si effettuano solo tre buchi nel torace del paziente, nel buco centrale si introduce una telecamera per la scopia nel buco superiore e inferiore due introduttori bipolari quindi uno con polo positivo e l'altro con polo negativo per catetere che vanno uno in vena cava superiore e l'altro in vena cava inferiore, si uniscono a formare un tutt'uno e una volta introdotti dei cateteri speciali che raggiungono la zona desiderata da ablare, si crea come un risucchio della parete da ablare che rimane come INTRAPPOLATA come se fosse in una scatola, si emette radiofrequenza a circa 70° e in tal modo facendo scorrere i cateteri si ottiene il completo isolamento sia interno che esterno delle vene polmonari da questo il nome di BOX LESION.
Questa tecnica ablativa può essere utilizzata come abbiamo detto precedentemente ANCHE per la fibrillazione atriale PERSISTENTE E PERMANENTE in entrambi i casi dato che il responsabile maggiore è l'ingrandimento atriale l'ablazione ibrida verrà estesa sia alle vene polmonari sia al substrato atriale.
C'è da dire inoltre che a volte gli inconvenienti possono capitare e anche in questo caso l'ablazione potrebbe non riuscire, in rari casi il grasso a livello posteriore del cuore può rappresentare un problema soprattutto in pazienti obesi poichè il grasso non permette il completo isolamento e quindi l'ablazione può fallire.
L'unica complicazione che è stata segnalata è un'iniziale PERICARDITE poichè quando si va ad ablare il substrato atriale si crea un'infiammazione del pericardio che va curata con antiinfiammatori.
I NUOVI ANTICOAGULANTI ORALI
I NUOVI ANTICOAGULANTI ORALI ( NAO )
I nuovi anticoagulanti orali (NAO), inibitori diretti della trombina (dabigatran) e inibitori diretti del fattore Xa (rivaroxaban, apixaban), negli studi di fase III hanno dimostrato almeno una non inferiorità nei confronti del warfarin nella riduzione del rischio tromboembolico della fibrillazione atriale (FA). Inoltre hanno comportato una riduzione dei sanguinamenti fatali, in particolare delle emorragie intracraniche. I NAO presentano il vantaggio di essere somministrabili in dosi fisse giornaliere e di non richiedere il monitoraggio periodico dell’ international normalized ratio (INR). Negli anziani pertanto i NAO potrebbero diventare in futuro il trattamento anticoagulante di scelta.
Numerosi trial clinici randomizzati e successive metanalisi hanno dimostrato che la terapia anticoagulante orale (TAO) con warfarin è altamente efficace nella prevenzione primaria e secondaria dell’ictus nei pazienti affetti da FA1,2. Con il warfarin si ottiene una riduzione del rischio di ictus del 64%3, controbilanciata però da un aumento delle emorragie maggiori, pari all’1.2% per anno nei trial, ma molto maggiore nei registri. Il timore delle emorragie costituisce la remora principale per l’utilizzo della TAO, soprattutto nei pazienti anziani, per i quali esiste sicuramente un aumentato rischio emorragico connesso alla TAO4. Questo spiega l’apparente paradosso che i pazienti ultra75enni, esposti ad un maggior rischio di ictus in presenza di FA, sono proprio quelli meno trattati. Complessivamente, soltanto la metà dei pazienti affetti da FA sono effettivamente trattati con warfarin e nei soggetti anziani il sottoutilizzo è ancora maggiore5.
Sono stati recentemente pubblicati i risultati dello studio multicentrico osservazionale ATA-AF6, in cui sono stati valutati, nel periodo compreso tra maggio e luglio 2010, i pazienti con FA afferiti a 164 cardiologie e 196 reparti di medicina interna, rappresentativi in termini di distribuzione geografica della realtà ospedaliera italiana. I pazienti arruolati avevano un’età mediana di 77 anni e nel 47% dei casi erano femmine. Per la prevenzione del rischio tromboembolico la TAO è stata prescritta soltanto nel 58.8% dei casi, ed in assenza di correlazione con il CHA 2DS2-VASc score. La prescrizione della TAO è risultata influenzata maggiormente dall’età (66.2% nei pazienti di età ≤75 anni vs 53.1% nei pazienti di età >75 anni, p<0.0001) (Figura 1), dal tipo di FA (64.3% nei casi di FA permanente, 69.6% nei casi di FA persistente e soltanto 37.4% nei pazienti con FA parossistica, p<0.0001) e dalla strategia terapeutica adottata (63.2% in caso di strategia di controllo della frequenza vs 59.7% in caso di strategia di controllo del ritmo, p<0.0001).
In letteratura, peraltro, è stato dimostrato che nei pazienti affetti da FA il beneficio clinico netto che si ottiene con la TAO aumenta con l’età7. Nel 2007 lo studio BAFTA ha dato ulteriore supporto all’efficacia e alla sicurezza del warfarin nel trattamento di 973 pazienti con FA di età ≥75 anni (età media 81.5 ± 4.2 anni)8. L’incidenza annua di eventi tromboembolici è risultata dell’1.8% nei pazienti trattati con warfarin e del 3.8% in quelli trattati con aspirina, con un rischio relativo (RR) di 0.48 (p=0.003), in assenza di un significativo aumento del rischio emorragico. L’incidenza annua di emorragie maggiori, infatti, non è stata diversa tra i due trattamenti, rispettivamente 1.9% per il warfarin e 2.0% per l’aspirina. In uno studio prospettico italiano pubblicato nel 2011 la sicurezza del warfarin è stata inoltre dimostrata in un’ampia casistica (4093 pazienti) di ultra80enni in TAO per FA o per tromboembolia venosa seguiti nei Centri di Sorveglianza della TAO 9. È stato riportato un rischio annuo di emorragie maggiori dell’1.87% e di emorragie fatali dello 0.27%. Pertanto, l’età avanzata di per sé non deve essere considerata una controindicazione alla TAO negli anziani con FA. Recentemente, uno studio nord-americano ha documentato che l’impiego di warfarin in pazienti con FA di età >70 anni si associa ad una riduzione di mortalità (hazard ratio 0.58, p<0.001), in assenza di sanguinamenti maggiori (hazard ratio 0.73, p=0.229) 10. Se la TAO viene accuratamente condotta, con l’esclusione dei soggetti ad elevato rischio emorragico, anche negli ultra75enni con FA i benefici risultano ampiamente superiori ai rischi.
In letteratura, è peraltro riportata in molti pazienti una inadeguata qualità dell’anticoagulazione. Anche attuando frequenti monitoraggi ed aggiustamenti della dose, i pazienti in trattamento con warfarin risultano per oltre un terzo del tempo al di fuori del target terapeutico (tempo nel range terapeutico, TTR)11. Una metanalisi di studi pubblicati tra il 2005 ed il 2008 ha evidenziato che complessivamente i pazienti con FA sono solo per il 55% del loro tempo con INR all’interno del TTR12. Dati italiani recentemente pubblicati di registri amministrativi dimostrano che nel nostro Paese il TTR medio dei pazienti warfarin-naïve è 47.9%, mentre quello dei pazienti warfarin-experienced è 56.3% (Tabella 1). Entrambi questi valori rimangono al di sotto del valore considerato soddisfacente (60%)13.
In questo scenario si colloca l’introduzione dei NAO, studiati e sviluppati a seguito dei noti limiti della TAO con warfarin (lento inizio d’azione, risposta non prevedibile, stretta finestra terapeutica, necessità di monitoraggio routinario dei fattori della coagulazione e numerose interazioni farmacologiche ed alimentari), e del conseguente sottoutilizzo nei pazienti affetti da FA.
I NUOVI ANTICOAGULANTI ORALI
I NAO sono rappresentati dagli inibitori diretti orali della trombina (dabigatran) e del fattore Xa (rivaroxaban e apixaban), la cui efficacia e sicurezza sono state testate dapprima nella prevenzione della trombosi venosa profonda e dell’embolia polmonare in pazienti sottoposti a chirurgia elettiva dell’anca o del ginocchio.
Dal 2009 ad oggi sono stati pubblicati tre studi di fase III nei quali i NAO sono stati confrontati con il warfarin nella prevenzione del rischio tromboembolico associato alla FA (Figura 2).
Dabigatran
Il dabigatran è un inibitore diretto orale reversibile della trombina, caratterizzato da una biodisponibilità del 6.5%, un’emivita plasmatica di 12-17h ed eliminazione renale per l’80%. Nello studio RE-LY14-16 il dabigatran è risultato non inferiore al warfarin a dosi aggiustate (INR 2.0-3.0) al dosaggio di 110 mg bid (RR 0.91, p<0.001) e superiore al warfarin a dosi aggiustate al dosaggio di 150 mg bid (RR 0.66, p<0.001) nella riduzione del rischio tromboembolico di 18 113 pazienti affetti da FA non valvolare. L’impiego di dabigatran 150 mg si è inoltre associato ad una riduzione statisticamente significativa dell’incidenza di ictus ischemico. Per quanto riguarda l’endpoint di sicurezza l’incidenza di sanguinamenti maggiori rispetto al warfarin è risultata inferiore con il dosaggio 110 mg bid (RR 0.80, p=0.003) e sovrapponibile con il dosaggio 150 mg bid. L’incidenza di sanguinamenti cerebrali correlata all’utilizzo di dabigatran è risultata significativamente inferiore (riduzione del 60% circa) rispetto a quella in corso di warfarin, indipendentemente dal dosaggio del farmaco e dall’età dei pazienti. È da sottolineare il fatto che all’interno dello studio RE-LY più di un terzo dei pazienti (in totale, 7258) aveva un’età >75 anni. In tale sottogruppo il dabigatran al dosaggio di 150 mg bid ha comportato un rischio emorragico superiore a quello del warfarin (5.10 vs 4.37%/anno), mentre al dosaggio di 110 mg bid il rischio di sanguinamenti è risultato sovrapponibile a quello del warfarin (4.43 vs 4.37%/anno, p<0.001) (Figura 3) 17. Gli stessi dati sono stati confermati in un’analisi post-hoc sui pazienti “very elderly” (ovvero ultra80enni; in totale, 3016) dello studio RE-LY, rispettivamente ≥80 anni (17%), ≥85 anni (4%) e ≥90 anni (0.4%)18. Il rischio annuo di emorragie maggiori associato all’impiego di dabigatran 110 mg bid è risultato 5.25%, sovrapponibile a quello del warfarin (4.7%), mentre quello associato all’uso di dabigatran 150 mg bid è risultato superiore a quello del warfarin (6.24%). Pertanto, negli anziani è raccomandato l’utilizzo della posologia di 110 mg bid. Un dato assolutamente importante in proposito è la sovrapponibilità dei risultati del confronto dabigatran-warfarin nei pazienti warfarin-naïve ed in quelli warfarin-experienced, rappresentati in percentuali simili all’interno del braccio dei pazienti randomizzati al warfarin19. In una successiva sottoanalisi dello studio RE-LY, il dabigatran è inoltre risultato almeno non inferiore al warfarin anche nel sottogruppo di pazienti con pregresso ictus o attacco ischemico transitorio (TIA), popolazione nella quale risulta particolarmente rilevante la riduzione dell’ictus emorragico in confronto al warfarin20.Rivaroxaban
Il rivaroxaban è un inibitore diretto orale del fattore Xa con elevata biodisponibilità (80%) ed emivita plasmatica di 7-11h, che presenta il vantaggio, rispetto agli altri NAO, della monosomministrazione giornaliera. È metabolizzato per due terzi nel fegato e per un terzo è eliminato per via renale.
L’efficacia del rivaroxaban nella FA è stata valutata nello studio ROCKET AF21 nel quale 14 171 pazienti con FA sono stati randomizzati a ricevere rivaroxaban 20 mg/die, ridotto a 15 mg/die nei pazienti con insufficienza renale moderata (clearance della creatinina 30-49 ml/min), oppure warfarin (INR 2.0-3.0). I pazienti con FA inclusi nello studio ROCKET AF erano caratterizzati da un profilo di rischio tromboembolico maggiore rispetto a quelli dello studio RE-LY (CHADS2 score ≥3 nell’87 vs 32% nel RE-LY, e pregresso ictus o TIA nel 55 vs 20% nel RE-LY). Il rivaroxaban è risultato non inferiore al warfarin, con un tasso annuale di ictus ed embolia sistemica del 2.12 vs 2.42% (p<0.001) riportato con il warfarin. Gli eventi emorragici correlati all’impiego del NAO sono risultati numericamente sovrapponibili a quelli del warfarin, ma con una significativa riduzione dei sanguinamenti fatali (0.2 vs 0.5%/anno, p=0.003) e cerebrali (0.5 vs 0.7%/anno, p=0.02). Il rivaroxaban inoltre, in considerazione della ridotta quota di eliminazione per via renale, si è dimostrato particolarmente sicuro nei pazienti affetti da insufficienza renale di grado moderato ( clearance della creatinina 30-49 ml/min), che rappresenta la comorbosità più frequente nel soggetto anziano22.
Apixaban
L’apixaban è un inibitore diretto orale del fattore Xa a rapido assorbimento, con biodisponibilità del 66%, escreto soltanto per il 25% per via renale.
È stato dapprima testato vs aspirina nello studio AVERROES (studio di superiorità) in pazienti affetti da FA non eleggibili per la TAO. Lo studio è stato prematuramente interrotto per l’evidenza di superiorità, peraltro attesa, di apixaban al dosaggio di 5 mg bid nella riduzione degli eventi tromboembolici rispetto all’aspirina a vari dosaggi (81-324 mg/die), con un tasso di emorragie maggiori ed in particolare intracraniche sovrapponibile per i due tipi di trattamento23.
In seguito, nell’ARISTOTLE l’apixaban è stato confrontato al dosaggio di 5 mg bid con il warfarin a dosi aggiustate (INR 2.0-3.0) in pazienti affetti da FA e con un fattore di rischio per l’ictus ischemico24. Nel trial, il NAO veniva testato ad un dosaggio ridotto (2.5 mg bid) nei pazienti ad elevato rischio emorragico (ovvero in presenza di due o tre dei seguenti criteri: età ≥80 anni, peso ≤60 kg, creatinina ≥1.5 mg). Apixaban è risultato superiore al warfarin nella prevenzione di ictus ed embolie sistemiche (1.27 vs 1.60%/anno, p=0.01). Tale superiorità è stata documentata anche per l’endpoint di sicurezza, con una riduzione significativa delle emorragie maggiori (2.13 vs 3.09%/anno, p<0.001) e delle emorragie cerebrali (0.33 vs 0.80%/anno, p<0.001). L’efficacia e la sicurezza dell’apixaban sono risultate ancora più significative nel sottogruppo di pazienti affetti da FA con precedente ictus o TIA, come dimostra una sottoanalisi dello studio ARISTOTLE, in cui la riduzione annua del rischio di eventi tromboembolici rispetto al warfarin è risultata essere 0.77% (vs 0.22% nei soggetti affetti da FA senza ictus/TIA anamnestico) 25.
Edoxaban
Il panorama dei NAO si arricchirà ulteriormente, nel corso dei prossimi anni, di una nuova molecola, l’edoxaban, un inibitore diretto del fattore Xa con elevata biodisponibilità (62%), escreto per il 50% per via renale che coniuga il vantaggio della monosomministrazione (caratteristica propria anche a rivaroxaban) con la possibilità dell’aggiustamento del dosaggio (caratteristica propria anche a dabigatran).
Entro il 2013 sono attesi i risultati dello studio di fase III ENGAGE AF-TIMI 4826, nel quale circa 20 000 pazienti con FA ad elevato rischio tromboembolico (CHADS2 score ≥2) sono stati randomizzati a ricevere edoxaban 30 mg/die o 60 mg/die, confrontato con il warfarin a dosi aggiustate (INR 2.0-3.0) con l’obiettivo di dimostrarne la non inferiorità.
Nonostante i risultati siano ancora attesi e, quindi, non sia possibile al momento un confronto di efficacia e sicurezza rispetto agli altri NAO, per il duplice, contemporaneo vantaggio della monosomministrazione e della possibilità di aggiustamento posologico, potrebbe rappresentare un’opzione terapeutica particolarmente indicata negli anziani, nei quali queste caratteristiche potrebbero garantire maggiore aderenza e migliore personalizzazione del trattamento anticoagulante in base alle comorbosità presenti.
VANTAGGI DEI NUOVI ANTICOAGULANTI ORALI
In aggiunta alla dimostrazione di ampia efficacia e sicurezza, i NAO si distinguono dal “vecchio” warfarin per la non necessità di monitoraggio dei livelli di scoagulazione e per la possibilità di essere assunti in dosi giornaliere fisse. Questi due aspetti risultano particolarmente rilevanti nel soggetto anziano, in cui frequentemente la TAO non viene prescritta non per reali controindicazioni cliniche, bensì per difficoltà logistiche nel monitoraggio periodico dell’INR o per possibilità di scarsa compliance alla terapia, come riportato nel trial AVERROES23. Con l’impiego dei NAO, pertanto, verrebbero meno le più frequenti motivazioni di non utilizzo del warfarin e si andrebbe a colmare almeno in parte il sottotrattamento dei pazienti affetti da FA27.
Nei soggetti anziani, inoltre, i NAO potrebbero rappresentare l’anticoagulante di scelta in considerazione della significativa riduzione del rischio emorragico che comportano, ed in particolare dei sanguinamenti cerebrali e fatali. Recentemente, inoltre, è stato reso noto mediante un comunicato della Food and Drug Administration, che nel mondo reale i sanguinamenti secondari all’impiego di dabigatran negli anziani sono risultati meno frequenti di quelli osservati nel RE-LY28.
I pazienti anziani sono esposti infatti ad una maggior incidenza di eventi emorragici, dipendente dall’età e dalle comorbosità. A riguardo, in un recente studio di popolazione canadese è stata documentata un’incidenza di eventi emorragici in corso di trattamento con warfarin nettamente superiore a quella riportata nei trial clinici randomizzati. In una casistica di circa 125 000 soggetti ultra66enni affetti da FA, durante un follow-up di 10 anni, l’incidenza annua di emorragie è risultata 3.8% (vs 1-3% riportato nei trial). Come già noto in letteratura, è stato confermato che il maggior numero di eventi emorragici si è verificato nei primi 30 giorni dall’inizio della TAO (incidenza annua per persona pari all’11.8%) 29.
Negli anziani, comunemente in polifarmacoterapia per le comorbosità, i NAO presentano anche il vantaggio di avere poche interferenze farmacologiche con farmaci peraltro di non frequente impiego. Occorre infatti cautela nell’impiego dei NAO in associazione a potenti induttori o inibitori della glicoproteina P, quali claritromicina, verapamil, ketoconazolo e ciclosporina. Le concentrazioni plasmatiche di rivaroxaban ed apixaban inoltre possono essere influenzate dai forti induttori o inibitori del citocromo P450 isoforma CYP3A4 29.
Infine, i NAO risultano farmaci ampiamente maneggevoli data la breve emivita, con inizio e termine d’azione rapidi, che ne consentono la sospensione in caso di intervento chirurgico senza necessità di embricazione con eparina a basso peso molecolare.
POTENZIALI CRITICITÀ DEI NUOVI ANTICOAGULANTI ORALI
Attualmente, nonostante il grande entusiasmo per l’introduzione nella pratica clinica dei NAO, rimangono da definire:
a) un sistema di monitoraggio laboratoristico in caso di eventi emorragici o trombotici;
b) la gestione dei sanguinamenti, data la mancanza di un antidoto per questi nuovi farmaci;
c) un sistema di sorveglianza dei pazienti per valutare l’aderenza alla terapia.
Dopo la somministrazione dei NAO, diversi test coagulativi risultano alterati, con un prolungamento del tempo di protrombina, del tempo di tromboplastina parziale attivato (aPTT), del tempo di trombina e del tempo di ecarina30. Questi ultimi due parametri sono i più affidabili per la determinazione quantitativa del livello di anticoagulazione ottenuto con dabigatran. Nei casi in cui i test quantitativi non siano disponibili, per dabigatran può essere utilizzato l’aPTT. Se quest’ultimo risulta >80 s, il rischio emorragico è elevato. L’intensità di scoagulazione ottenuta con rivaroxaban ed apixaban invece sembra correlare in maniera soddisfacente con le misurazioni del tempo di protrombina.
Per la gestione degli eventi emorragici, occorre fare delle distinzioni in base all’entità del sanguinamento. Se è lieve, disponendo di farmaci con breve emivita, è sufficiente procrastinare l’assunzione della dose successiva o sospendere temporaneamente il trattamento per arrestare il sanguinamento. In caso di emorragia di grado moderato/severo, deve essere mantenuta la volemia con infusione di liquidi e trasfusioni di plasma fresco congelato. Se il paziente è in terapia con dabigatran, possono essere utili la somministrazione di carbone attivato, per ridurne l’assorbimento gastrointestinale soprattutto se l’ultima dose è stata assunta entro le 2h precedenti, e l’emodialisi per rimuovere il farmaco dal circolo, data la consistente quota di escrezione per via renale (80%). In caso di eventi emorragici che potrebbero risultare fatali, per antagonizzare l’effetto anticoagulante viene consigliata la somministrazione di concentrati di complessi protrombinici (attivati e non attivati) e di fattore VII attivato ricombinante 31.
Infine, la criticità verosimilmente più rilevante per l’impiego dei NAO è rappresentata dall’identificazione di un sistema di sorveglianza clinica dei pazienti. La mancanza della necessità di un monitoraggio periodico dei parametri emocoagulativi può comportare il rischio di una sorveglianza non adeguata del paziente anticoagulato, che potrebbe non essere consapevole dell’importanza e dei rischi della nuova terapia. Pertanto, si rendono indispensabili:
a) un colloquio informativo con il paziente al momento della prima prescrizione dei NAO;
b) controlli clinici periodici (almeno ogni 3 mesi) per valutare la compliance, per registrare eventuali eventi emorragici anche minori non segnalati, e per verificare variazioni delle terapie concomitanti e modifiche significative nel tempo del rischio emorragico (comparsa di deficit cognitivi, insorgenza di nuove comorbosità, ecc.);
c) controlli ravvicinati della funzionalità renale. Negli anziani sono infatti particolarmente frequenti variazioni della creatinina per concomitante assunzione di farmaci interferenti e per tendenza alla disidratazione26.
Infine, il costo rappresenta un’altra potenziale criticità per l’impiego dei NAO nella comune pratica clinica, pur considerando il risparmio del monitoraggio laboratoristico periodico dell’INR necessario per il warfarin. Numerose analisi di costo-efficacia sono però risultate favorevoli all’utilizzo dei NAO, in considerazione della riduzione dei costi, che si ottiene anche attraverso la riduzione degli eventi tromboembolici ed emorragici32,33. Un’analisi di budget impact, recentemente pubblicata, che ha preso in considerazione in diversi scenari clinici il costo del dabigatran, il costo del monitoraggio dell’INR e quello degli eventi tromboembolici, ha confermato che nel nostro Paese l’impiego di dabigatran è economicamente sostenibile, consentendo perfino un risparmio per il Sistema Sanitario Nazionale nella gestione dei pazienti affetti da FA a partire dal secondo anno di trattamento rispetto all’utilizzo del warfarin 34.
PAZIENTI ELEGGIBILI AI NUOVI ANTICOAGULANTI ORALI
Nei pazienti con FA di nuovo riscontro ed indicazione alla TAO (warfarin-naïve), i NAO si collocano come l’anticoagulante di scelta anche nella popolazione degli anziani e molto anziani35. Indicazioni prioritarie per i NAO sono rappresentate dai pazienti con difficoltà logistiche nell’effettuare il monitoraggio laboratoristico periodico o con pregresso ictus ischemico o emorragia intracranica.
Diverso è lo scenario dei pazienti con FA già in TAO (warfarin-experienced). Se il controllo della TAO è affidabile con un TTR soddisfacente (≥60%) può essere ragionevole non attuare uno switch immediato ai NAO, tranne che per espressa volontà del paziente.
Esiste tuttavia un significativo numero di pazienti, soprattutto anziani, nei quali la qualità della TAO non è soddisfacente (TTR <60%) per compliance non ottimale o per difficoltà logistiche nella gestione della terapia. Inoltre, non è raro il verificarsi di eventi tromboembolici o emorragici correlati ad ampie fluttuazioni dell’INR o anche in corso di TAO con INR in range terapeutico. In questi pazienti, che complessivamente costituiscono circa un terzo dei pazienti in TAO, è ragionevole lo switch dal warfarin ai NAO. Infine, la prescrizione dei NAO sarà sicuramente raccomandata in quell’ampia categoria di pazienti affetti da FA attualmente esclusi dalla TAO per un elevato rischio emorragico, oppure trattati con aspirina nell’erronea convinzione che la terapia antiaggregante comporti un rischio emorragico inferiore a quello della TAO36.
CONCLUSIONI
I NAO rappresentano una delle più importanti innovazioni terapeutiche dell’ultimo decennio. Complessivamente, come effetto di classe hanno dimostrato un’efficacia almeno non inferiore rispetto al warfarin nella riduzione degli eventi tromboembolici nei pazienti affetti da FA non valvolare e, allo stesso tempo, sono risultati sicuri, con una riduzione statisticamente significativa delle emorragie fatali, in particolare di quelle intracraniche (Figura 4)14,15,21,24. Il loro impiego, inoltre, si associa ad un trend di riduzione della mortalità. Pertanto negli anziani, che presentano un elevato rischio tromboembolico ed emorragico, rappresentano il trattamento anticoagulante di scelta, in considerazione anche delle difficoltà che l’utilizzo del warfarin presenta in questa categoria di pazienti.
RIASSUNTO
La terapia anticoagulante orale (TAO) con inibitori della sintesi di fattori della coagulazione K-dipendenti riduce significativamente il rischio tromboembolico nei pazienti con fibrillazione atriale (FA), ma comporta un aumento del rischio emorragico. Nei pazienti anziani è stato dimostrato che il beneficio clinico netto della TAO aumenta con l’età, nonostante un rischio emorragico maggiore. Pur con queste evidenze, nella pratica clinica si assiste ad un sottoutilizzo della TAO. Inoltre, il tempo trascorso all’interno del range terapeutico non risulta soddisfacente, con conseguente aumento del rischio tromboembolico ed emorragico. Il sottoutilizzo e la qualità subottimale del trattamento anticoagulante risultano più frequenti nei pazienti anziani. In questi, potrebbe essere particolarmente vantaggioso l’impiego dei nuovi anticoagulanti orali, che non richiedono monitoraggio sistematico del grado di anticoagulazione e, a parità – o in alcuni studi con superiorità – dell’effetto protettivo contro gli eventi cardioembolici, sembrano garantire anche un minor rischio di eventi emorragici maggiori.
Parole chiave. Anticoagulanti orali; Anziani; Fibrillazione atriale; Rischio emorragico; Rischio tromboembolico.
ARTICOLO TRATTO DAL GIORNALE ITALIANO DI CARDIOLOGIA
RHYTHMIA - Un'apparecchiatura per una più precisa localizzazione del punto di insorgenza delle aritmie
RHYTMIA
Sistema di cartografia cardiaca ad elevata precisione
Desidero portare a conoscenza di tutti un articolo pubblicato sul quotidiano “Nice Matin” del 27 giugno 2015 (a firma di Nancy Cattan), corredato della relativa traduzione
Aritmia cardiaca: Monaco arricchisce il suo arsenale
In primo piano: Localizzare con estrema precisione i tessuti implicati nelle turbe del ritmo per migliorarne ulteriormente il trattamento: la provocazione di Rhythmia
Al mondo esistono solo 17 apparecchi di questo tipo. Uno di essi è installato nel Servizio di Cardiologia del Centro ospedaliero “Principessa Grace” (HPG) di Monaco, diretto dal Prof. Nadir Saoudi. “Rhythmia è un sistema di cartografia cardiaca ad altissima definizione che permette un’analisi di precisione ineguagliata delle turbe del ritmo cardiaco,in un tempo molto più breve di prima” riassume il cardiologo.
Tutto inizia con l’introduzione cuore (attraverso la vena femorale) di una specie di “ombrellino” - privo di tessuto – composto da 8 stecche, dotate ciascuna di 8 elettrodi. Ossia 64 ricettori capaci di registrare l’attività cardiaca nei più piccoli recessi del muscolo
Una misura di attività elettrica localizzata
“Ogni volta che un catetere tocca la parete del cuore, sul computer appare un’immagine in 3D che permette di localizzare con estrema precisione l’attività elettrica,in particolare a livello degli atri (cavità cardiache, NdR), la cui immagine è subito ricostruita. Si dispone così di indicazioni preziose sui tessuti implicati nelle turbe del ritmo, come un flutter (ritmo regolare ma rapido degli atri, NdR) o una fibrillazione atriale (contrazione rapida e disordinata degli atri che impedisce al cuore di funzionare normalmente e di far circolare bene il sangue nel corpo, NdR). E questa precisione ci permette di trattare ancora più efficacemente le turbe del ritmo”.
La posta è ancora più alta, sapendo che la cronicità di queste aritmie cardiache favorisce la formazione di coaguli e rappresenta dunque un pericolo potenziale di incidente vascolare, cerebrale o cardiaco.
Per ora, il costo molto elevato della procedura (1) e l’esperienza necessaria per la sua esecuzione limitano le indicazioni di Rhythmia alla diagnosi delle turbe del ritmo su pazienti ben mirati: “Quelli che hanno sviluppato un’aritmia in seguito ad un intervento cardiaco, in particolare di chirurgia valvolare, o dopo l’insuccesso di un’ablazione intracardiaca classica”.
Ad oggi una trentina di casi hanno beneficiato di questo nuovo sistema al CHPG. “Ne abbiamo parlato recentemente a Boston nell’ambito del Congresso Heart Rhytm Association” si rallegra il Prof. Saoudi (2).
E non c’è nessun dubbio: le performances di Rhythmia sono tali che a breve dovranno beneficiarne tutti.
- (1) L’apparecchio è stato finanziato grazie a dei donatori e l’esame è rimborsato senza costi per
i pazienti.
- (2) La sua équipe fa parte di un gruppo internazionale di studio delle aritmie con questo
apparecchio, creato da poco.
____________________________________________________________
se lo desideri puoi scaricare una copia pdf di questo articolo poco sotto.
LE EXTRASISTOLE VENTRICOLARI
LE EXTRASISTOLE VENTRICOLARI
Le extrasistole ventricolari riconosciute anche come BATTITI ECTOPICI VENTRICOLARI (BEV) o BATTITI PREMATURI VENTRICOLARI essendo ECTOPICI non nascono nel NIDO SENO ATRIALE ma in questo caso al di sotto della BIFORCAZIONE DEL FASCIO DI HIS nel SETTO INTERVENTRICOLARE situato tra i due ventricoli
Le extrasistole ventricolari possono presentarsi in modo SPORADICO. IRREGOLARE ma anche in forma CONTINUATIVA oppure REGOLARE allorché verranno definite ALLORITMICHE.
I BEV possono presentarsi in forma BIGEMINA se all'elettrocardiogramma compaiono tra due battiti sinusali, in forma TRIGEMINA tra tre battiti sinusali e così via.
Le extrasistole ventricolari possono presentarsi anche in COPPIA ovvero due extrasistole vicine in TRIPLETTA o tre extrasistole ravvicinate, QUADRUPLE quattro extra ravvicinate, mentre se si presentano da cinque in su vengono definite SALVE VENTRICOLARE.
Le extrasistole ventricolari possono essere di due morfologie ovvero MONOMORFE ad una morfologia oppure POLIMORFE a più morfologie.
Le extrasistole ventricolari molto spesso non nascendo nel normale sistema di conduzione ma bensì nella parete libera del ventricolo in questione all'ecg si presentano con un complesso ventricolare QRS largo maggiore di 0,12 msec ma capita che a volte essi si presentino con un QRS STRETTO nel momento in cui il battito prematuro insorga all'interno del sistema di conduzione.
Con l'asse elettrico del QRS del battito ectopico ventricolare e' possibile stabilire l' esatta sede d'insorgenza dell'extrasistola infatti con un asse rivolto verso l'alto si presuppone l' insorgenza verso l'apice cardiaco mentre con l'asse rivolto verso il basso si presuppone l' insorgenza verso il TRATTO DI EFFLUSSO.
Dalla morfologia dell'extrasistola e' possibile stabilire se il ventricolo coinvolto e' quello destro oppure il sinistro infatti se un battito ectopico ventricolare si presenta a tipi di blocco di branca sinistra la sua origine sarà dal ventricoli destro mentre se e' a tipo di blocco di branca destra l' origine sarà dal ventricolo sinistro.
Diverse sono le cause che portano alla formazione delle extrasistole, le più accreditate sono: l' AUTOMATISMO ANORMALE ovvero la formazione dell'impulso anomalo, il RIENTRO ovvero la formazione di un circuito di rientro che fa muovere un impulso su se stesso e l' ATTIVITÀ TRIGGERATA ovvero un impulso scatenante.
Nel normale automatismo le cellule atte alla formazione e alla conduzione dell'impulso elettrico si trovano nel NODO SENO ATRIALE NEL NODO ATRIO VENTRICOLARE NEL FASCIO DI HIS CON LE SUE DIRAMAZIONI E NELLE FIBRE DEL PURKINJE.
La maggior parte di queste cellule possiede una bassa frequenza di scarica e intervengono solo nel momento in cui il pacemaker fisiologico ovvero il nodo seno atriale ha una frequenza molto bassa o il suo impulso non riesce ad arrivare ai ventricoli.
Nell'AUTOMATISMO ANORMALE invece queste cellule preposte si trovano nel miocardio comune sia atriale che ventricolare.
Nel normale automatismo la normale attivazione dell'impulso e' a carico degli IONI SODIO mentre in quello ANORMALE a carico degli IONI CALCIO.
Per quanto riguarda il RIENTRO, le extrasistole ventricolari possono essere innescate da dei microrientri che possono formarsi vicino alle diramazioni della rete del Purkinje oppure in un tessuto fibroso al cui interno ci sia la presenza di aree vitali.
Esistono delle oscillazioni del potenziale di membrana che si verificano durante o subito dopo il potenziale d'azione che possono essere responsabili di battiti ectopici ventricolari in tal caso si usa il termine di ATTIVITA' TRIGGERATA.
i POSTPOTENZIALI dipendono dal battito precedente e le aitmie legate a questo meccanismo hanno sempre una causa scatenante. Esistono due tipi di POSTPOTENZIALI divisi in PRECOCI E TARDIVI, le aritmie che insorgono per POSTPOTENZIALI TARDIVI sono quveelle da INTOSSICAZIONE DIGITALICA, IPOKALIEMIA, IPOCALCEMIA E IPOMAGNESIEMIA o ingestione di alte dosi di CAFFEINA.
La diagnosi elettrocardiografica delle extrasistole ventricolari si basa sull'individuazione di battiti prematuri con un coplesso QRS largo, tuttavia va escluso che un battito largo sia dovuto ad un'extrasistola sopraventricolare condotta con aberranza a causa di un blocco di branca destra quindi occorre analizzare attentamente 'attivazione dell'onda P ( se visibile ) il rapporto tra onda P e complesso QRS e la morfologia del QRS ma uno degli elementi che chiarisce maggiormente se si tratta di un BATTITO ECTOPICO VENTRICOLARE O DI UN BATTITO ECTOPICO SOPRAVENTRICOLARE è la PAUSA che ne consegue, che sarà COMPENSATORIA PER LE EXTRASISTOLE VENTRICOLARI E non compensatoria per LE EXTRASISTOLE SOPRAVENTRICOLARI.
FIBRILLAZIONE ATRIALE E MAZE
 La fibrillazione atriale è un’aritmia, ovvero un disturbo del ritmo cardiaco, in cui l’impulso elettrico, invece di procedere ordinatamente dal nodo senoatriale, in cui nasce spontaneamente, insorge da focolai multipli, situati negli atri, che ne risultano caoticamente attivati.
La fibrillazione atriale è un’aritmia, ovvero un disturbo del ritmo cardiaco, in cui l’impulso elettrico, invece di procedere ordinatamente dal nodo senoatriale, in cui nasce spontaneamente, insorge da focolai multipli, situati negli atri, che ne risultano caoticamente attivati.
A questo punto, il movimento degli atri, anziché essere ritmico e regolare (80 battiti per minuto, mediamente) diviene vermicolare, con le singole fibre muscolari che si contraggono molto rapidamente, ma disordinatamente, ognuna per proprio conto. Di fatto, dunque, gli atri risultano nel complesso immobili, privi di funzione propulsiva, per cui il sangue fluisce nei ventricoli per gravità, senza esservi spinto attivamente, mentre nelle auricole, strutture piramidali a larga base dì impianto, una per atrio, anch’esse prive di contrattilità, si formano facilmente coaguli che possono guadagnare (soprattutto a sinistra) la circolazione sistemica, attraverso il ventricolo sinistro, come emboli, provocando ictus.
La contrazione dei ventricoli è irregolare e avviene quando gli impulsi riescono ad attraversare il nodo atrioventricolare, irregolarmente, con frequenza variabile.
Le immagini seguenti, tratte per lo più da “Netter’s Cardiology”, oltre che dal web esemplificano il rapporto tra fibrillazione atriale e trattamento chirurgico della stessa.
________________________________________________________________________
Nell’immagine soprastante, il cuore inserito nel torace, in visione anteriore, allo specchio. L’apice è in basso, a sinistra (destra dell’osservatore); la faccia anteriore (parete anteriore del ventricolo sinistro) è sormontata a destra (sinistra dell’osservatore) dall’auricola destra, di colore blu scuro. Dalla base, in alto, si staccano da destra a sinistra (dalla sinistra alla destra dell’osservatore), i grossi vasi: la vena cava superiore, blu (che porta il sangue all’atrio destro), l’aorta, rossa (che porta il sangue a tutto il corpo), l’arteria polmonare, blu, che porta il sangue ai polmoni. Sulla radice dell’arteria polmonare, poggia l’apice dell’auricola sinistra (rossa).
________________________________________________________________________
Nel disegno a fianco, il cuore in visione anteriore e sezione  longitudinale, rimosse le pareti anteriori delle 4 camere e i grossi vasi. In alto a destra (sinistra dell’osservatore), l’atrio destro (rosa), con il nodo seno atriale (blu) nello spessore del tetto, gli sbocchi delle vene cave superiore e inferiore (blu) e il nodo atrioventricolare (in giallo, sul pavimento) che prosegue nel sistema di conduzione atrioventricolare (giallo) che si dirama nei ventricoli, le camere inferiori, a forma di cono rovesciato. Nell’atrio sinistro (in alto a sinistra, ovvero a destra dell’osservatore) l’atrio sinistro con gli sbocchi delle 4 vene polmonari (rosse), di cui solo 3 qui rappresentate, che portano il sangue dai polmoni.
longitudinale, rimosse le pareti anteriori delle 4 camere e i grossi vasi. In alto a destra (sinistra dell’osservatore), l’atrio destro (rosa), con il nodo seno atriale (blu) nello spessore del tetto, gli sbocchi delle vene cave superiore e inferiore (blu) e il nodo atrioventricolare (in giallo, sul pavimento) che prosegue nel sistema di conduzione atrioventricolare (giallo) che si dirama nei ventricoli, le camere inferiori, a forma di cono rovesciato. Nell’atrio sinistro (in alto a sinistra, ovvero a destra dell’osservatore) l’atrio sinistro con gli sbocchi delle 4 vene polmonari (rosse), di cui solo 3 qui rappresentate, che portano il sangue dai polmoni.
________________________________________________________________________
 L’immagine a sinistra riproduce la conduzione normale dell’impulso elettrico che nasce nel nodo senoatriale, si propaga ordinatamente negli atrii, fino al nodo atrioventricolare e di qui ai ventricoli.
L’immagine a sinistra riproduce la conduzione normale dell’impulso elettrico che nasce nel nodo senoatriale, si propaga ordinatamente negli atrii, fino al nodo atrioventricolare e di qui ai ventricoli.
L’impulso origina spontaneamente a intervalli precisi, normalmente determina un ritmo regolare, detto appunto sinusale per il nodo di partenza e si trasmette alle pareti muscolari delle 4 camere, che si contraggono in sequenza, prima gli atri e poi i ventricoli, per spingere il sangue in aorta, a sinistra e arteria polmonare, a destra.
________________________________________________________________________
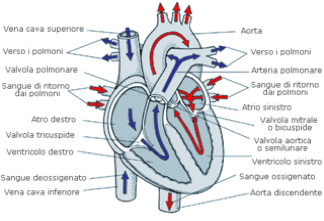
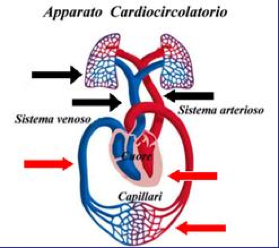
Attraverso le vene cave, il sangue fluisce dagli organi periferici all’atrio destro. Di qui, attraverso la valvola tricuspide, al ventricolo destro. Quindi, attraverso la valvola polmonare, all’arteria polmonare. Quindi: polmoni, vene polmonari, atrio sinistro, valvola mitrale, ventricolo sinistro, valvola aortica, aorta, arterie periferiche, organi periferici, capillari, vene periferiche, vene cave, atrio destro.
_____________________________________________________________________________________________________________________
Nelle immagini seguenti, la relazione tra fibrillazione atriale e maze.
Tutto il cuore, si tratti di tessuto di conduzione o fibre muscolari, è costituito da potenziali focolai di origine di impulsi elettrici di scarica spontanea, propagabile, solitamente silenti e inibiti dall’attività del nodo seno atriale.
Nella fibrillazione atriale, i focolai elettrici atriali sono innumerevoli, attivi, prendono il sopravvento sul nodo seno atriale, si propagano in ogni direzione e determinano una contrazione caotica degli atri, che risultano funzionalmente fermi e l’irregolarità nella contrazione ritmica dei ventricoli.

Nella prima immagine, in alto a sinistra, le pareti degli atri, con gli sbocchi delle 2 vene cave (blu), delle 4 vene polmonari (rosse), il nodo seno atriale (verde), l’auricola destra, l’auricola sinistra, il sistema di conduzione atrio-ventricolare (bianco).
La seconda immagine, in alto a destra, raffigura la parete posteriore del cuore, in particolare dell’atrio sinistro, con gli sbocchi delle 4 vene polmonari.
La terza immagine, in basso a sinistra, illustra le linee prodotte dai tagli e dalle successive suture (cosiddetto taglia e cuci), con la creazione di cicatrici impermeabili al passaggio di elettricità, volte a parcellizzare l’atrio, creando piccole isole, all’interno di un labirinto (maze, in inglese), in cui l’impulso segua una via obbligata che, dal nodo seno atriale, lo indirizzi al sistema di conduzione atrioventricolare, indisturbato dagli eventuali focolai ectopici attivi, ma finalmente isolati.
Nell’immagine in basso a destra, il risultato dell’intervento di taglia e cuci su entrambi gli atri, con l’asportazione delle auricole, sedi di focolai ectopici anch’esse, ma, soprattutto, di formazione di coaguli che posso raggiungere la circolazione sistemica, con possibilità di ictus, o polmonare, con possibilità, meno frequente, di embolia polmonare.
Poiché nella stragrande maggioranza dei casi, i focolai, detti ectopici perché siti in altro luogo rispetto al nodo del seno, segnapassi naturale e fisiologico, si trovano in corrispondenza degli sbocchi delle vene polmonari, si è visto che l’isolamento delle stesse è spesso sufficiente ad ablare ovvero eliminare la fibrillazione atriale. Ove così non fosse, occorrerebbe aggiungere altre linee di sutura.
I cardiologi iniziarono così a mimare le linee di sutura dall’interno del cuore, anziché dall’esterno, mediante cateteri a radiofrequenza cicatrizzante da dirigere contro le pareti interne dell’atrio sinistro, con passaggio attraverso vena femorale, vena cava inferiore, atrio destro, perforazione del setto interatriale e raggiungimento dell’atrio sinistro (cateterismo cardiaco).
Nel frattempo, i cardiochirurghi riducevano sempre più le dimensioni dell’accesso al cuore (chirurgia mini invasiva), passando dalla sternotomia, alla minitoracotomia, alla toracoscopia addirittura, con il risultato di accessi puntiformi a consentire l’isolamento delle vene polmonari con una pinza a radiofrequenza e l’esclusione dell’auricola sinistra mediante posizionamento di semplici clips, senza tagliare, né cucire il cuore, pure creando le necessarie cicatrici.
Le immagini seguenti illustrano diverse tecniche di accesso al cuore.
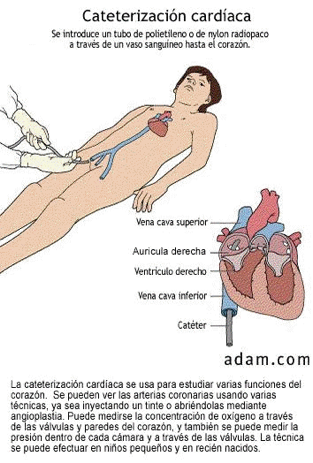
STERNOTOMIA
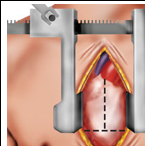
MINITORACOTOMIA
TORACOSCOPIA
questo articolo è stato scritto da Dott. Antonio Lazzari
LE EXTRASISTOLE SOPRAVENTRICOLARI
Le extrasistole sopraventricolari riconosciute anche come battiti ectopici sopraventricolari o BESV, sono degli impulsi prematuri o anticipati che nascono in zone diverse negli atri o nella giunzione atrioventricolare. Possono presentarsi in forma sporadica o ripetitiva solo in rari casi viene previsto l'utilizzo di beta bloccanti ma possono comunque innescare aritmie sopraventricolari come la fibrillazione atriale.
Le extrasistole sopraventricolari possono insorgere per un'attività triggerata, per un esaltato automatismo o più semplicemente per un circuito di rientro.
Esse rappresentano un'attivazione atriale anticipata che può insorgere come un accoppiamento ( la classica sensazione di doppio battito ) oppure con un intervallo post extrasistolico la cui pausa non è compensatoria.
Essendo un battito diverso da quello sinusale, l'onda P che ne consegue, sarà diversa sia come morfologia che come asse dalla P sinusale e talvolta è possibile identificare, tramite un'attenta analisi del tracciato elettrocardiografico, la sede esattada cui proviene l'extrasistola.
A volte può risultare difficoltosa l'individuazione dell'extrasistola poichè essa può coincidere con l'onda T del battito precedente.
La conduzione dei battiti ectopici sopraventricolari ai ventricoli può essere normale, aberrante a causa di un rallentamento di conduzione intraventricolare oppure bloccata con la conseguente pausa.
Le extrasistole sopraventricolari possono presentarsi in soggetti con cuore sano ma anche in caso di processi infiammatori, ischemici o più semplicemente per abuso di sostanze stimolanti come alcol tabacco e caffeina.
Studi condotti a metà degli anni 90 in Francia da Haiissaguerre hanno permesso di identificare come alcuni focus ectopici ovvero siti sensibili di innesciìo di extrasistole sopraventricolari come ad esempio l'ostio delle vene polmonari fossero in grado di innescare e mantenere non solo la fibrillazione atriale ma anche il flutter e altre aritmie in cui è previsto un circuito di rientro.
La comparsa di BESV subito dopo la cardioversione elettrica può suffragare una recidiva di aritmia a breve.
Recentemente è stato dimostrato che un numero maggiore di 32 BESV all'ora è fortemente predittorio di recidive di fibrillazione atriale ad un mese.
Nel sesso femminile la sede di origine delle extrasistole sopraventricolari in grado di innescare fibrillazione atriale è la vena cava superiore probabilmente per un'esaltata attività parasimpatica ma altre sedi possono essere il legamento di Marshall, la parete posteriore dell'atrio sinistro o l'ostio del seno coronarico.
La possibilità di identificare la sede esatta dei battiti ectopici può essere un valido aiuto alla terapia ablativa della fibrillazione atriale, se si è certi che tale aritmia sia causata da esse.



